Document de principes
L’évaluation des enfants et des adolescents ayant un retard global du développement et un trouble du développement intellectuel
Affichage : le 27 mars 2026
Auteur(s) principal(aux)
Scott McLeod MD, Anne Kawamura MD, Angela Orsino MD, Société canadienne de pédiatrie, Comité de la santé mentale et des troubles du développement
Résumé
Les prestataires de soins aux enfants jouent un rôle essentiel auprès des enfants ayant un retard global du développement et un trouble de développement intellectuel. Ce rôle englobe la détection précoce des problèmes de développement, l’orientation des familles tout au long du processus diagnostique, la coordination des soins avec d’autres prestataires de soins aux enfants et avec les enseignants et les mesures pour garantir l’accès aux interventions appropriées. Une évaluation approfondie de l’histoire médicale, un examen physique approfondi et l’amorce d’une exploration génomique, en fonction des indications cliniques et des ressources disponibles, sont les piliers de l’évaluation de ces enfants. Les tests métaboliques ne sont recommandés que dans des situations particulières, qui sont décrites brièvement.
Mots-clés : évaluation; planification préalable des soins; tests génétiques; troubles du développement
Définitions
Le retard global du développement (RGD) est un trouble neurodéveloppemental caractérisé par des retards importants dans au moins deux domaines du développement, y compris la motricité fine ou globale, l’élocution et le langage, le fonctionnement cognitif, social et personnel et le fonctionnement adaptatif[1]. Le diagnostic de RGD est réservé aux enfants de moins de cinq ans, qui sont trop jeunes pour effectuer des tests cognitifs officiels (p. ex., des tests intellectuels standardisés comme l’échelle d’intelligence de Wechsler pour enfants [WISC] ou l’échelle d’intelligence Standford-Binet)[1]. Le RGD est diagnostiqué d’après une combinaison d’observations cliniques et d’évaluations développementales structurées. Il est défini de différentes façons dans les publications scientifiques, et aucun score numérique universel ou escompté obtenu à l’aide des outils d’évaluation du développement n’a de valeur diagnostique[1][2]. En revanche, le trouble de développement intellectuel (TDI) se caractérise à la fois par des limites du fonctionnement intellectuel et du comportement adaptatif, toutes deux confirmées par une évaluation clinique standardisée et par la capacité de l’enfant à répondre aux critères socioculturels d’autonomie personnelle et de responsabilité sociale[1]. Puisque le RGD est un diagnostic réservé aux enfants de moins de cinq ans, les prestataires de soins aux enfants doivent envisager une évaluation officielle du TDI pendant l’enfance ou l’adolescence afin de s’assurer que les mesures de soutien se poursuivent et de garantir l’admissibilité aux services destinés aux adultes.
Les psychologues et les rapports officiels classent souvent le TDI en fonction de sa gravité, qui reflète souvent l’importance du soutien dont la personne a besoin ou dont elle pourrait profiter. Le DSM-5-TR le classe également d’après sa gravité, mais le pédiatre peut généralement adopter une démarche plus pratique des soins s’il s’attarde à un plan individuel et à des soins et un soutien personnalisés pour optimiser le fonctionnement quotidien et la qualité de vie de l’enfant ou de l’adolescent.
La prévalence
On observe un RGD dans une proportion estimative de 1 % à 3 % des enfants de moins de cinq ans dans le monde, mais presque partout, sa détection et son diagnostic sont influencés par des facteurs sociétaux (p. ex., l’accès à des programmes d’intervention précoce et à des ressources de soins spécialisées), par les attitudes culturelles envers les troubles de développement[3] et par les déterminants sociaux de la santé (p. ex., l’insécurité alimentaire, car les carences nutritionnelles peuvent en moduler les manifestations)[4].
Les données de prévalence du TDI sont demeurées plutôt stables au fil du temps. Selon une estimation mondiale récente, la prévalence atteignait 1,5 % dans les pays à revenu élevé et 3,1 % dans l’ensemble du monde, ce qui laisse croire qu’elle est beaucoup plus marquée dans les pays à revenu faible ou modéré[5]. Cependant, dans certaines populations ayant un diagnostic de trouble du spectre de l’autisme, la proportion des enfants qui présentent également un TDI a diminué[6].
Le rôle des prestataires de soins aux enfants
Les prestataires de soins aux enfants sont bien placés pour détecter tôt les retards de développement, ce qui est essentiel pour améliorer l’évolution à long terme des enfants et des adolescents ayant un RGD ou un TDI[7]. Même s’il n’est pas recommandé de procéder à un dépistage transversal unique du développement auprès de la population générale[8], une surveillance longitudinale à l’aide d’outils comme le Relevé postnatal Rourke au Canada, conjointement avec des évaluations du développement plus ciblées, est recommandée au pays et ailleurs[9].
En cas de présomption de retard de développement, les prestataires de soins aux enfants orientent les familles tout au long du processus d’évaluation, ce qui inclut l’histoire développementale, médicale et familiale. Pour évaluer l’histoire du développement, ils peuvent utiliser des ressources déjà en place, comme les tableaux des étapes du développement et les outils de dépistage accessibles avant de diriger l’enfant vers des collègues pour obtenir une évaluation plus précise et standardisée. L’intégration d’évaluations relatives à la discipline et une compréhension clinique éclairée de la capacité de développement de chaque enfant contribuent à poser le diagnostic de RGD. Les prestataires de soins aux enfants jouent un rôle essentiel pour expliquer aux familles ce diagnostic et le processus d’orientation vers des spécialistes. Pour ce faire, ils synthétisent les résultats de multiples sources, puis les transmettent aux parents et aux autres proches. De tels conseils aident les parents à comprendre le profil de développement de leur enfant, atténuent l’anxiété et éclairent les futures étapes de prise en charge et d’intervention.
Les prestataires de soins aux enfants jouent également un rôle essentiel de collaboration avec l’équipe soignante de l’enfant ou de l’adolescent, lequel peut inclure, pour le suivi des deux affections, un pédiatre du développement, un neurologue, un généticien et des spécialistes de la santé connexes. Une communication et une coordination efficaces peuvent être capitales pour la planification et l’adoption de soins complets qui répondront aux besoins de l’enfant ou de l’adolescent. De plus, les prestataires de soins aux enfants peuvent assurer la liaison avec les éducatrices à la petite enfance et les enseignants pour s’assurer d’aménager des mesures d’accommodements appropriées qui répondront aux besoins de développement de chaque enfant ou adolescent, tout en préconisant Ies services d’éducation spécialisée et Ies plans d’intervention individuels, nécessaires. Les prestataires de soins aux enfants doivent également aborder les problèmes de santé et de comportement avec les familles et les orienter vers des ressources communautaires et des groupes d’entraide.
Les pronostics
Le pronostic du RGD est un domaine complexe et évolutif qui repose sur les données probantes en médecine et sur les publications scientifiques récentes. Selon une étude rétrospective canadienne qui remonte à 2009, les résultats cognitifs des enfants ayant reçu un diagnostic de RGD étaient très vastes; 73 % avaient un quotient intellectuel d’au moins 70, ce qui suppose qu’une forte proportion ne respectait pas les critères de TDI malgré un diagnostic antérieur de RGD[10]. Cette étude comportait des limites notables, mais a établi que, même si la motricité fine et les capacités de langage expressif étaient solidement associées à la performance cognitive, les capacités de langage réceptif n’étaient pas un fort prédicteur de problèmes cognitifs plus tard dans la vie[10]. D’après une étude rétrospective plus récente, la corrélation entre les scores d’évaluation développementale précoces et le fonctionnement intellectuel par la suite était plus solide : les enfants qui obtenaient un résultat d’au moins deux écarts types sous la moyenne des échelles de développement mentale de Griffiths à l’âge de deux à trois ans présentaient une probabilité d’obtenir des résultats dans la plage de la déficience intellectuelle (quotient intellectuel total ne dépassant pas 70) de 86 % sur l’échelle d’intelligence Stanford-Binet 5 à l’âge de quatre à six ans[11]. Des données probantes aussi mitigées laissent supposer que le pronostic de RGD peut toujours tirer profit de tests propres à ce domaine, d’une surveillance à long terme et d’un suivi en vue de soins personnalisés et d’un plan individuel.
Les étiologies possibles
Le RGD et le TDI sont associés à diverses étiologies qui peuvent être classées largement en facteurs prénatals, périnatals et postnatals, décrits au tableau 1[12]. Il est à souligner que l’exposition prénatale à l’alcool ou les facteurs de risque révélés par l’anamnèse ne remettent pas en cause la nécessité d’une évaluation étiologique complète ni d’une évaluation développementale chez les enfants et les adolescents ayant un RGD ou un TDI.
|
Tableau 1. Les étiologies du retard global du développement et du trouble de développement intellectuel |
|
|
Moment de l’exposition |
Exemples |
|
Période prénatale |
Origine infectieuse - Infection congénitale (cytomégalovirus, herpes simplex, rubéole, syphilis, toxoplasmose, varicelle, Zika) Système nerveux central - Holoprosencéphalie, polymicrogyrie Origine génétique ou métabolique - Syndrome de Prader-Willi, erreurs innées du métabolisme Expositions toxiques - Éthanol, substances illicites, médicaments tératogènes |
|
Période périnatale |
Prématurité Encéphalopathie hypoxo-ischémique |
|
Période postnatale |
Origine infectieuse - Méningite, encéphalite Traumatisme crânien Expositions toxiques - Plomb Origine métabolique - Hypoglycémie Négligence Carences nutritionnelles - Fer, vitamine B12 |
Information tirée de la référence 12
Une démarche d’évaluation en cabinet
Le RGD et le TDI sont répandus en pédiatrie. L’évaluation initiale inclut une anamnèse et un examen physique ciblés, conformément au tableau 2.
|
Tableau 2. L’anamnèse et l’examen physique du retard global du développement et du trouble de développement intellectuel |
|
|
ANAMNÈSE |
|
|
Préoccupations |
|
|
Histoire périnatale |
Grossesse - Maladies de la mère - Exposition à des médicaments ou à des substances psychoactives - Signes d’infection congénitale (p. ex., fièvre, éruption) - Observations anormales à l’échographie ou au dépistage prénatal Histoire de naissance - Âge gestationnel (corrigé en cas de naissance prématurée) - Poids, taille et périmètre crânien à la naissance - Scores d’APGAR - Complications pendant l’accouchement et besoin de réanimation Période néonatale - Admission en soins intensifs néonatals - Ictère, convulsions, infections (p. ex., méningite, encéphalite), problèmes métaboliques (p. ex., hypoglycémie), traumatisme - Dépistages du nouveau-né, particulièrement chez les nouveaux arrivants au Canada |
|
Évaluation développementale |
|
|
Histoire familiale |
Idéalement, tenir compte de trois générations, y compris :
|
|
Histoire sociale |
S’informer :
|
|
Histoire médicale |
Passé
Évaluation
|
|
EXAMEN PHYSIQUE |
|
|
Observations développementales et fonctionnelles
Paramètres de croissance (taille, poids, périmètre crânien)
Tête et cou
Appareil cutané
Appareil cardiovasculaire
Système abdominal
Appareil neurologique
Appareil locomoteur
|
|
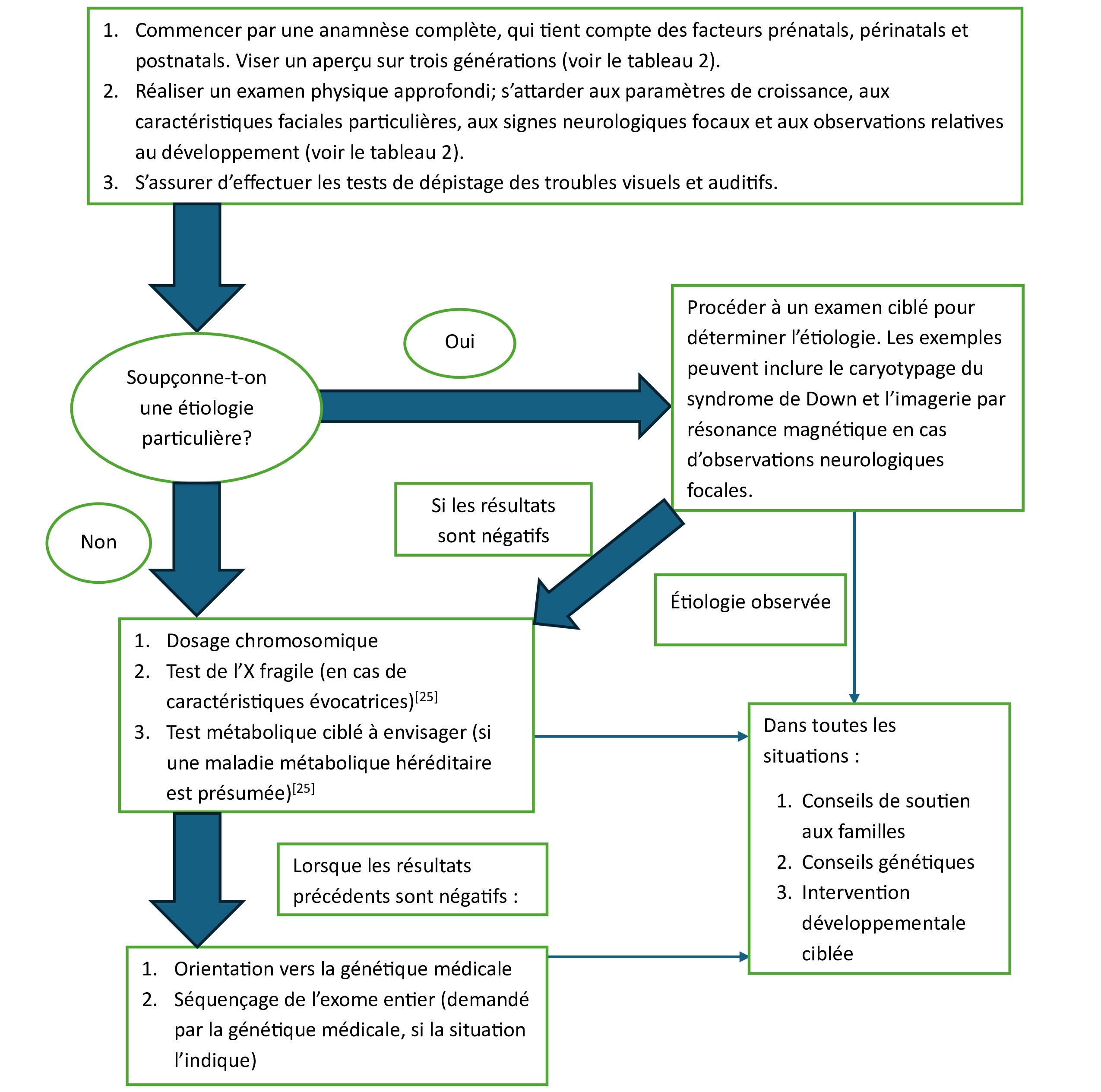
Les prestataires de soins pour enfants peuvent avoir besoin d’effectuer un bilan plus approfondi, conformément à la figure 1.
Figure 1. L’évaluation du retard global du développement et du trouble de développement intellectuel en fonction de l’anamnèse, des examens physiques et d’un examen à deux niveaux
Le test de dépistage des troubles auditifs
La perte auditive congénitale touche de un à trois nouveau-nés sur 1 000 naissances vivantes et constitue une observation isolée dans de nombreux cas. Chez les enfants atteints d’une perte auditive syndromique, environ 20 % présentent également des troubles du développement (p. ex., RGD ou trouble du spectre de l’autisme), craniofaciaux (p. ex., fente palatine), neurologiques (p. ex., épilepsie) ou d’autres troubles systémiques (p. ex., insuffisance cardiaque ou rénale ou déficience visuelle)[13]. Environ 50 % des cas de surdité qui découlent d’une perte auditive congénitale sont d’origine génétique, et environ la moitié des cas non syndromiques sont attribuables à une mutation génique de la connexine 26[13]. Il est capital de vérifier l’audition dans le cadre de l’évaluation étiologique du RGD et du TDI, particulièrement lorsqu’elle est jumelée à une histoire familiale détaillée sur trois générations. Un examen auditif de suivi doit faire partie de l’évaluation du RGD et du TDI, même lorsque le dépistage des troubles auditifs était normal chez les nouveau-nés[14].
Le dosage du fer
Selon un document de principes antérieur de la Société canadienne de pédiatrie, la ferritine sérique et l’hémogramme pouvaient constituer les premiers examens de laboratoire (premier niveau) pour évaluer le RGD ou le TDI[15]. Une étude longitudinale phare réalisée au Costa Rica a révélé que les enfants atteints d’une carence en fer chronique pendant la première enfance obtenaient des résultats de huit à neuf points plus bas sur les échelles cognitives que ceux dont l’apport précoce en fer était normal, et leur risque développemental se maintenait plus tard au cours de leur vie, même après le traitement[16]. Une récente étude canadienne a corroboré ces résultats[17]. Le dosage de la ferritine est recommandé chez les enfants dont les familles semblent aux prises avec l’insécurité alimentaire ou présentent les facteurs de risque suivants : alimentation au biberon prolongée, ingestion d’une grande quantité de lait de vache par jour, ingestion d’une faible quantité de viande ou indice de masse corporelle plus élevé que celui des camarades[17]. Le dépistage tardif de ces enfants (en présence d’anémie ou de symptômes) réduit les avantages du traitement par suppléments de fer et des changements aux habitudes alimentaires, car la carence en fer chronique demeure un risque développemental au fil du temps.
Les tests de la fonction thyroïdienne
Le dépistage métabolique du nouveau-né permet de détecter une hypothyroïdie congénitale qui, si elle demeure non traitée, peut entraîner une déficience du fonctionnement neurologique et un retard de croissance. Au moins deux études menées dans des contextes où l’apport en iode est suffisant n’ont révélé aucune association entre les taux de thyréostimuline (thyréotrophine) des nouveau-nés et les résultats cognitifs[18][19]. Le dosage de la thyréostimuline pour déterminer l’étiologie du RGD ou du TDI n’est probablement pas nécessaire dans le cadre du dépistage métabolique du nouveau-né au Canada, mais peut être indiqué pour évaluer les enfants ou les adolescents qui viennent d’arriver au Canada ou dont les signes cliniques sont évocateurs d’une hypothyroïdie.
Le dosage du plomb
Les enfants peuvent être exposés au plomb s’ils ingèrent des articles non comestibles (pica). Une faible exposition chronique est clairement associée à une neurotoxicité, à des problèmes d’attention et à des résultats plus faibles aux tests de quotient intellectuel[20]. Au Canada, la surveillance active de la plombémie a réduit les concentrations de plomb sérique de 38 % entre 2007 et 2009 et entre 2018 et 2019[20]. Les concentrations de plomb dans les populations autochtones qui habitent dans les réserves sont similaires à celles de la population générale[20]. Le dosage systématique du plomb n’est pas recommandé pour évaluer le RGD ou le TDI, mais peut être envisagé en présence de pica.
La neuro-imagerie et la neurophysiologie
Dans une étude auprès d’enfants et d’adolescents ayant un RGD ou un TDI, des modifications à l’imagerie par résonance magnétique cérébrale ont été constatées chez 38 % de ceux qui ne présentaient pas de signes ou de symptômes neurologiques ni d’étiologie diagnostique confirmée[21]. Des anomalies suscitaient un diagnostic étiologique de RGD ou de TDI dans 7,9 % de cette population[21]. Des lésions cérébrales à l’imagerie par résonance magnétique sont plus prévalentes chez les enfants et les adolescents qui présentent un retard moteur marqué, conjointement avec un déficit visuel et auditif, des anomalies des nerfs crâniens et des réflexes anormaux[22]. La neuro-imagerie doit être envisagée en présence d’observations neurologiques focales, de microcéphalie et de régression développementale, mais ne devrait pas être systématique, notamment parce qu’elle peut exiger une sédation et qu’il faut éviter l’exposition inutile à une anesthésie générale.
L’électroencéphalographie permet de mesurer l’activité électrique de groupes de neurones dont les décharges sont simultanées. La prévalence d’anomalies observées à l’électroencéphalographie est plus élevée dans les cas de RGD et de TDI, mais celles-ci sont fortement associées à des résultats anormaux à l’imagerie par résonance magnétique, à des modifications génomiques et à des facteurs de risque périnatals de RGD et de TDI[23]. Bien que l’électroencéphalographie soit utile pour confirmer les syndromes épileptiques et électrocliniques, les données probantes sont insuffisantes pour en établir l’intérêt comme examen de première ligne du RGD ou du TDI.
Les examens métaboliques et génétiques
Lorsque les manifestations cliniques laissent supposer une étiologie particulière, il faudrait procéder à des tests génétiques ciblant l’affection présumée. Jusqu’à tout récemment, en 2018, une série de tests métaboliques de premier niveau, du nom de protocole TIDE (Treatable Intellectual Disability Endeavor, ou initiative pour la déficience intellectuelle traitable), était recommandée pour établir l’étiologie du RGD et du TDI[15], mais des études subséquentes semblent démontrer que ce protocole est associé à un rendement diagnostique plus faible qu’on le croyait auparavant. Des modifications à ce régime de tests[24] ont été recommandées depuis, comme suit : 1) ne dépister que les enfants ayant un RGD ou un TDI qui présentent des manifestations neurologiques ou métaboliques supplémentaires (p. ex., hypotonie marquée, convulsions réfractaires, régression du développement) et 2) procéder au dosage des acides aminés dans le plasma, de l’homocystéine totale, des acides organiques des urines et des métabolites de la créatinine dans les urines, mais exclure les autres tests proposés auparavant (p. ex., profil de l’acylcarnitine, lactate, ammoniaque, cuivre et céruloplasmine)[24]. Les examens métaboliques ne sont plus recommandés chez les enfants et les adolescents qui ne présentent pas de manifestations neurologiques ou métaboliques.
Le Collège canadien des généticiens médicaux a publié une déclaration de principe en 2023 pour adopter une démarche plus ciblée des examens biochimiques et métaboliques en général et suggérer une nouvelle façon de dépister le syndrome de l’X fragile en particulier. Plutôt que de dépister le syndrome de l’X fragile dès le départ, parmi les tests diagnostiques de premier niveau des personnes ayant un RGD, un TDI ou un trouble du spectre de l’autisme, le Collège recommande désormais des tests en fonction de l’anamnèse et de l’examen physique (seulement en présence de manifestations cliniques ou d’une histoire familiale évocatrices)[25]. Ce document recommande toujours le microdosage chromosomique comme test de premier niveau pour l’évaluation génomique d’un enfant ou d’un adolescent ayant un RGD ou un TDI[25]. Ce test permet de détecter les variations du nombre de copies (de petites duplications ou de petites délétions du matériel génétique), qui représentent des altérations du nombre de copies de gènes particuliers ou de segments d’ADN[25].
Le séquençage de l’exome entier est une démarche de séquençage de prochaine génération qui consiste à analyser les régions de codage de protéines (exons) de tous les gènes connus du génome humain. Puisque les exons représentent de 1 % à 2 % du génome, mais renferment environ 85 % des variants pathogènes connus, le séquençage de l’exome entier constitue une solution économique à fort rendement par rapport au séquençage du génome humain pour déterminer les étiologies génétiques des troubles neurodéveloppementaux, y compris le RGD et le TDI[25]. Le Collège canadien des généticiens médicaux recommande le séquençage de l’exome entier comme test génétique de deuxième niveau chez les personnes ayant un RGD ou un TDI lorsque le test de premier niveau (p. ex., le microdosage chromosomique) n’en a pas établi l’étiologie[24]. Le rendement diagnostique du séquençage de l’exome entier du RGD et du TDI, qui varie entre 26 % et 31 %, repose sur les observations tirées de vastes études cliniques[26][27]. Lorsque le test inclut le séquençage de l’exome entier des deux parents biologiques en plus de celui de l’enfant, le rendement diagnostique augmente comparativement à la démarche qui se limite au cas de référence[25]. Comme l’accès aux conseils et aux tests génétiques s’améliore au fil du temps, le séquençage de l’exome entier pourrait devenir un test de premier niveau, conformément aux recommandations de l’American Academy of Pediatrics[28]. Cependant, pour le confort du patient, il faut limiter les prises de sang liées aux examens génétiques et déposer les échantillons dans des banques d’acide désoxyribonucléique, dans la mesure du possible.
Les soins de soutien
Même si la recherche de l’étiologie peut comporter des avantages particuliers pour les proches, tels qu’une meilleure compréhension des raisons qui expliquent les différences développementales, l’information sur la prise en charge et la surveillance des soins, la clarification du pronostic, l’orientation vers des groupes qui vivent la même affection et, dans certains cas, un meilleur accès à la recherche, il faudrait toujours prioriser le soutien des forces fonctionnelles de l’enfant ou de l’adolescent et les domaines dans lesquels il éprouve des besoins. Les prestataires de soins aux enfants peuvent se servir de la Classification internationale du fonctionnement de l’Organisation mondiale de la Santé pour orienter les soins pratiques et de soutien[29]. Cette classification répertorie les structures et les fonctions corporelles liées à l’évaluation médicale ciblée décrite plus haut, pour optimiser la santé générale. Mais surtout, elle priorise les activités du quotidien, qui peuvent être encouragées par des thérapies ciblées, comme l’ergothérapie pour soutenir le fonctionnement au quotidien (p. ex, hygiène et habillage) et l’orthophonie (y compris les stratégies de suppléance ou de remplacement à la communication) et insiste sur la participation, sous forme d’activités de loisirs adaptées afin de répondre aux besoins individuels[29]. Dans la mesure du possible, les enfants et les adolescents ayant un RGD ou un TDI devraient participer à la planification des soins et à la détermination des objectifs, conformément à leur développement et à leurs capacités.
Au-delà des capacités intrinsèques de l’enfant ou de l’adolescent, il faut tenir compte des facteurs personnels (y compris les valeurs familiales, les croyances et les préférences individuelles) au moment de recommander des services de soutien et des soins axés sur la famille. Les familles ont des points de vue particuliers sur le rôle des traitements, les objectifs fonctionnels et l’acceptabilité des interventions.
Les familles peuvent éprouver de la difficulté à comprendre quels services sont fournis par le gouvernement, car les programmes varient énormément d’une région à l’autre du Canada et peuvent être difficiles d’accès. Des processus de demande complexes, des critères d’admissibilité incohérents et des variations en fonction des régions sociosanitaires créent des obstacles importants pour les familles qui cherchent de l’aide. Les familles qui changent de région sociosanitaire doivent souvent reprendre le processus de demande de services de soutien, lequel peut être chronophage, fastidieux et perturbateur pour la continuité des soins. Dans la mesure du possible, les prestataires de soins aux enfants devraient envisager de diriger les familles vers des personnes pivots ou des services de travail social pour faciliter l’accès à un financement, des programmes thérapeutiques et des accommodements scolaires. De plus, les prises de position des prestataires de soins pour l’harmonisation des services dans les diverses provinces et les divers territoires favorisent des améliorations systémiques.
Conclusion
L’évaluation du RGD et du TDI est un processus continu et fondé sur des données probantes, qui s’adapte à mesure qu’émergent de nouvelles technologies diagnostiques. Alors que le dépistage génétique devient plus accessible et pourrait modifier les futures recommandations, les pratiques exemplaires actuelles demeurent ancrées dans une anamnèse un examen physique approfondis ainsi que des des examens ciblés. La collaboration entre prestataires de soins aux enfants facilite la recherche, garantit un enseignement uniforme de la médecine et améliore l’efficacité diagnostique. Au-delà du diagnostic, il est essentiel d’adopter une démarche axée sur les forces et sur la famille pour soutenir les enfants et les adolescents ayant un RGD ou un TDI.
Recommandations
- Soumettre tous les enfants chez qui on soupçonne un retard global du développement (RGD) ou un trouble de développement intellectuel (TDI) à une anamnèse et à un examen physique approfondis, conjointement avec des tests de dépistage visuels et auditifs.
- En cas de RGD ou de TDI inexpliqué, recommander une analyse du microdosage chromosomique comme examen de premier niveau.
- Envisager le dépistage du syndrome de l’X fragile en fonction des manifestations cliniques ou de l’histoire familiale (ou des deux) plutôt que de le systématiser chez tous les jeunes ayant un RGD ou un TDI.
- Après un diagnostic de RGD ou de TDI, personnaliser les mesures de soutien cliniques et éducationnelles selon les domaines à suppléer, conformément aux valeurs et aux objectifs familiaux.
- Harmoniser les programmes financés par le gouvernement, les provinces et les territoires pour contribuer à garantir la continuité des soins chez les enfants et les adolescents ayant un RGD ou un TDI.
- Prévoir un financement généreux pour la formation sur le séquençage de l’exome et son utilisation comme test diagnostique chez les enfants et les adolescents ayant un RGD ou un TDI, en raison de son fort rendement diagnostique et de son utilité clinique.
- Actualiser les structures de rémunération des prestataires de soins aux enfants (p. ex., les codes de facturation) pour reconnaître et rembourser le temps consacré à la coordination des soins, aux communications avec l’école et les autres professionnels de la santé (p. ex., orthophonistes, ergothérapeutes) et à la préparation des formulaires, entre autres tâches nécessaires pour prodiguer des soins appropriés et défendre les intérêts des enfants et des adolescents ayant un RGD ou un TDI.
Remerciements
Le comité de la pédiatrie communautaire et le comité de direction de la section de la pédiatrie du développement ont révisé le présent document de principes.
COMITÉ DE LA SANTÉ MENTALE ET DES TROUBLES DU DÉVELOPPEMENT DE LA SOCIÉTÉ CANADIENNE DE PÉDIATRIE (2025-2026)
Membres : Scott McLeod MD (président), Amy Ornstein MD (représentante du conseil), Natasha Saunders MD, Megan Thomas MBCHB, Ripudaman Minhas MD, Lester Liao MD, Man Ying Bernice Ho B. Sc. (membre résidente)
Représentants : Olivia MacLeod MD (Académie canadienne de psychiatrie de l’enfant et de l’adolescent), Angela Orsino MD (section de la pédiatrie du développement de la SCP), Leigh Wincott MD (section de la santé mentale de la SCP)
Auteurs principaux : Scott McLeod MD, Anne Kawamura MD, Angela Orsino MD
Financement
Aucun financement n’a été accordé pour la préparation du présent manuscrit.
Conflits d’intérêts potentiels
Le docteur Scott McLeod déclare avoir été rémunéré pour siéger au conseil d’administration d’Ipsen Biopharmaceuticals.
Les autres auteurs n’ont aucuns conflits d’intérêts à déclarer.
Références
- American Psychiatric Association. Manuel diagnostique et statistique des trouble mentaux – texte révisé, 5e édition. Elsevier Masson SAS, Issy-les-Moulineaux : APA, 2023.
- Mithyantha R, Kneen R, McCann E, Gladstone M. Current evidence-based recommendations on investigating children with global developmental delay. Arch Dis Child 2017;102(11):1071–6. doi : 10.1136/archdischild-2016-311271
- McKenzie K, Milton M, Smith G, Ouellette-Kuntz H. Systematic review of the prevalence and incidence of intellectual disabilities: Current trends and issues. Curr Dev Disord Rep 2016;3:104–15. doi : 10.1007/s40474-016-0085-7
- Bayoumi I, Parkin PC, Birken CS et coll.; TARGet Kids! Collaboration. Association of family income and risk of food insecurity with iron status in young children. JAMA Netw Open 2020;3(7):e208603. doi : 10.1001/jamanetworkopen.2020.8603
- Olusanya BO, Smythe T, Ogbo FA et coll. Global prevalence of developmental disabilities in children and adolescents: A systematic umbrella review. Front Public Health 2023;11:1122009. doi : 10.3389/fpubh.2023.1122009
- Shenouda J, Barrett E, Davidow AL et coll. Prevalence and disparities in the detection of autism without intellectual disability. Pediatrics 2023;151(2): e2022056594. doi : 10.1542/peds.2022-056594
- Guralnick MJ. Early intervention for children with intellectual disabilities: An update. J Applied Res Intellect Disabil 2017;30(2):211–29. doi : 10.1111/jar.12233
- Groupe d’étude canadien sur les soins de santé préventifs. Recommendations on screening for developmental delay. CMAJ 2016;188(8):579–87. doi : 10.1503/cmaj.151437
- Rowan-Legg A, Bayoumi I, Kwok B et coll. The 2020 Rourke Baby Record release: A time for reflection and looking forward. Paediatr Child Health 2021;26(5):283–6. doi : 10.1093/pch/pxaa135
- Riou EM, Ghosh S, Francœur E, Shevell MI. Global developmental delay and its relationship to cognitive skills. Dev Med Child Neurol 2009;51(8):600–6. doi : 10.1111/j.1469-8749.2008.03197.x
- Karyadiguna N, Berni C, Barnes EH et coll. Does pre-school developmental assessment agree with later intellectual assessment? A retrospective cohort study. J Paediatr Child Health 2023;59(8):962–7. doi : 10.1111/jpc.16428
- Aldosari AN, Aldosari TS. Comprehensive evaluation of the child with global developmental delays or intellectual disability. Clin Exp Pediatr 2024;67(9):435–46. doi : 10.3345/cep.2023.01697
- Gettelfinger JD, Dahl JP. Syndromic hearing loss: A brief review of common presentations and genetics. J Pediatr Genet 2018;7(1):1–8. doi : 10.1055/s-0037-1617454
- Bower C, Reilly BK, Richerson J, Hecht JL; comité de l’exercice et de la médecine ambulatoire, section d’otorhinolaryngologie et de chirurgie de la tête et du cou. Hearing assessment in infants, children, and adolescents: Recommendations beyond neonatal screening. Pediatrics 2023;152(3):e2023063288. doi : 10.1542/peds.2023-063288
- Bélanger SA, Caron J; comité de la santé mentale et des troubles du développement, Société canadienne de pédiatrie. L’évaluation de l’enfant ayant un retard global du développement ou un handicap intellectuel. Paediatr Child Health 2018;23(6):411–9. doi : 10.1093/pch/pxy099
- Lozoff B, Jimenez E, Hagen J et coll. Poorer behavioral and developmental outcome more than 10 years after treatment for iron deficiency in infancy. Pediatrics 2000;105(4):E51. doi : 10.1542/peds.105.4.e51
- Gingoyon A, Borkhoff CM, Koroshegyi C et coll. Chronic iron deficiency and cognitive function in early childhood. Pediatrics 2022;150(6):e2021055926. doi : 10.1542/peds.2021-055926
- Trumpff C, De Schepper J, Vanderfaeillie J et coll. No association between elevated thyroid-stimulating hormone at birth and parent-reported problem behavior at preschool age. Front Endocrinol (Lausanne) 2016;7:161. doi : 10.3389/fendo.2016.00161
- Wassie MM, Smithers LG, Yelland LN et coll. Associations between newborn thyroid-stimulating hormone concentration and neurodevelopment and growth of children at 18 months. Br J Nutr 2021;126(10):1478–88. doi : 10.1017/S0007114521000325
- Santé Canada. Le plomb dans la population canadienne. 2021. Ottawa, Ont. Le 14 décembre 2021 (consulté le 5 novembre 2025).
- Murias K, Moir A, Myers KA et coll. Systematic review of MRI findings in children with developmental delay or cognitive impairment. Brain Dev 2017;39(8):644–55. doi : 10.1016/j.braindev.2017.04.006
- Alamri A, Aljadhai YI, Alrashed A et coll. Identifying clinical clues in children with global developmental delay/intellectual disability with abnormal brain magnetic resonance imaging (MRI). J Child Neurol 2021;36(6):432–9. doi : 10.1177/0883073820977330
- Lee YJ, Jo YH, Choi SH et coll. Is electroencephalography useful in children with developmental delays but without overt seizures? Ann Child Neurol 2024;32(2):105–14. doi : 10.26815/acn.2024.00444
- Vallance H, Sinclair G, Rakic B, Stockler-Ipsiroglu S. Diagnostic yield from routine metabolic screening tests in evaluation of global developmental delay and intellectual disability. Paediatr Child Health 2020;26(6):344–8. doi : 10.1093/pch/pxaa112
- Carter MT, Srour M, Au PYB et coll.; Collège canadien des généticiens médicaux. Genetic and metabolic investigations for neurodevelopmental disorders: Position statement of the Canadian College of Medical Geneticists (CCMG). J Med Genet 2023;60(6):523–32. doi : 10.1136/jmg-2022-108962
- Yang Y, Muzny DM, Xia F et coll. Molecular findings among patients referred for clinical whole-exome sequencing. JAMA 2014;312(18):1870–9. doi : 10.1001/jama.2014.14601
- Retterer K, Juusola J, Cho MT et coll. Clinical application of whole-exome sequencing across clinical indications. Genet Med 2016;18(7):696–704. doi : 10.1038/gim.2015.148
- Rodan LH, Stoler J, Chen E, Geleske T; conseil sur la génétique. Genetic evaluation of the child with intellectual disability or global developmental delay: Clinical report. Pediatrics 2025;156(1):e2025072219. doi : 10.1542/peds.2025-072219
- Organisation mondiale de la Santé. International classification of functioning, disability and health (ICF). Genève, Suisse : OMS; 2025 (consulté le 5 novembre 2025).
Avertissement : Les recommandations du présent document de principes ne constituent pas une démarche ou un mode de traitement exclusif. Des variations tenant compte de la situation du patient peuvent se révéler pertinentes. Les adresses Internet sont à jour au moment de la publication.