Document de principes
La dyslipidémie chez les enfants : le diagnostic, l’évaluation et la prise en charge
Affichage : le 27 février 2026
Auteur(s) principal(aux)
Michael Khoury MD, Jean-Luc Bigras MD, Elizabeth A. Cummings MD, Kevin C. Harris MD M. Sc. S., Robert A. Hegele MD, Mélanie Henderson MD Ph. D., Katherine M. Morrison MD, Julie St-Pierre MD Ph. D., Peter D. Wong MD Ph. D., Brian W. McCrindle MD MHP ; Société canadienne de pédiatrie, Comité de la pédiatrie communautaire
Résumé
L’athérosclérose, qui se manifeste pendant l’enfance, est directement liée à la présence et à la gravité des facteurs de risque cardiovasculaires, y compris la dyslipidémie. La détection et la prise en charge rapides de la dyslipidémie pendant l’enfance peuvent ralentir l’évolution de l’athérosclérose et réduire le risque de future maladie cardiovasculaire, particulièrement chez les enfants atteints d’un trouble génétique qui les prédispose à la dyslipidémie (p. ex., l’hypercholestérolémie familiale qui, souvent, demeure non diagnostiquée). Les stratégies de dépistage existantes peuvent permettre de détecter les cas de dyslipidémie avec efficacité en pédiatrie, mais devraient être à la fois plus globales et adoptées plus tôt. Il est essentiel d’évaluer les causes secondaires de la dyslipidémie chez les enfants, y compris la prise de médicaments et les troubles systémiques. Les traitements de première ligne sont axés sur les modifications au mode de vie et à l’alimentation en fonction du phénotype de la dyslipidémie. Les indications relatives à la médication dépendent de la gravité de la dyslipidémie et de l’évaluation du risque cardiovasculaire individuel.
Mots-clés : athérosclérose; dyslipidémie; hypercholestérolémie familiale; hypertriglycéridémie; troubles lipidiques
L’athérosclérose, qui est le fondement biopathologique de la maladie cardiovasculaire (MCV) et se manifeste pendant l’enfance, est directement liée tant à la présence qu’à la gravité des facteurs de risque cardiovasculaires, comme la dyslipidémie[1][2]. Il est de plus en plus pressant de détecter et de prendre en charge la dyslipidémie tôt, particulièrement dans les populations à risque, telles que celles qui sont prédisposées à des dyslipidémies graves et permanentes à cause de troubles lipidiques congénitaux comme l’hypercholestérolémie familiale (HF). Pourtant, les taux de dépistage des lipides nécessaires à la détection de ces troubles demeurent faibles au Canada[3][4]. Le présent document de principes de la Société canadienne de pédiatrie incorpore une longue mise à jour des pratiques cliniques, publiée en anglais par la Société cardiovasculaire du Canada et l’Association canadienne de cardiologie pédiatrique en 2022[5]. Il propose une démarche pour détecter, évaluer et prendre en charge la dyslipidémie en pédiatrie et s’attarde au dépistage et au traitement précoces de l’HF.
Définitions, épidémiologie et génétique
La dyslipidémie, de plus en plus prévalente chez les jeunes du Canada, peut être d’origine congénitale, monogénique ou (de plus en plus) non génétique[6]. Les taux de lipoprotéines normaux, limites et anormaux en pédiatrie sont définis au tableau 1[7].
|
Tableau 1. Concentrations acceptables, limites élevées et élevées de lipides plasmatiques et de lipoprotéines à jeun* |
|||
|
Catégorie |
Acceptable |
Limite |
Anormal |
|
Cholestérol total |
<4,4 mmol/L |
De 4,4 à <5,2 mmol/L |
≥5,2 mmol/L |
|
Cholestérol à lipoprotéines de basse densité |
<2,8 mmol/L |
De 2,8 à <3,4 mmol/L |
≥3,4 mmol/L |
|
Cholestérol non à lipoprotéines de haute densité |
<3,10 mmol/L |
De 3,10 à <3,75 mmol/L |
≥3,75 mmol/L |
|
Triglycérides |
|||
|
0 à 9 ans |
<0,8 mmol/L |
De 0,8 à <1,1 mmol/L |
≥1,1 mmol/L |
|
10 à 19 ans |
<1,0 mmol/L |
De 1,0 à <1,5 mmol/L |
≥1,5 mmol/L |
|
Cholestérol à lipoprotéines de haute densité |
>1,2 mmol/L |
De 1,0 à 1,2 mmol/L |
<1,0 mmol/L |
|
*L’évaluation du bilan lipidique non à jeun convient au dépistage initial, mais les valeurs anormales doivent être confirmées par une reprise du bilan lipidique à jeun. Adapté et traduit de la référence[7] |
|||
Au total, 25 dyslipidémies monogéniques peuvent se manifester pendant l’enfance[8]. L’HF, qui est la plus courante, est une maladie héréditaire autosomique codominante[9]. La forme hétérozygote, dont la prévalence maximale est de un cas sur 90 habitants dans certaines régions du Québec et d’environ un cas sur 300 habitants dans le reste du Canada, touche toutes les ascendances[10]. L’HF est diagnostiquée soit par test génétique, soit à l’aide de critères phénotypiques[10]. Un seuil très élevé de cholestérol à lipoprotéines de basse densité (LDL-C) de 4,0 mmol/L a été proposé chez les enfants pour détecter une HF franche en présence d’une mutation génique causale confirmée. Cependant, une HF probable est envisagée au même seuil de LDL-C de 4,0 mmol/L lorsqu’un parent au premier degré présente un LDL-C élevé ou une MCV athéroscléreuse prématurée[11].
Il existe d’autres dyslipidémies primaires en pédiatrie : l’hypertriglycéridémie grave[12], l’hyperlipidémie combinée et des taux élevés de lipoprotéine (a). L’hypertriglycéridémie grave peut être causée par un trouble autosomique récessif (biallélique) associé à un fonctionnement réduit de la lipoprotéine lipase, de l’une de ses protéines activatrices ou de ses partenaires de liaison[12]. L’hyperlipidémie combinée, caractérisée par des triglycérides, un LDL-C et une apolipoprotéine B élevés, est très courante, mais généralement polygénique[12]. Des taux élevés de lipoprotéine (a) sont à forte base génétique et très peu influencés par des facteurs secondaires; ils entraînent une augmentation du risque cardiovasculaire[13][14].
Les dyslipidémies secondaires représentent un fardeau croissant en pédiatrie. Elles sont résumées dans la mise à jour originale des pratiques cliniques (voir le tableau 4, en anglais)[5]. La dyslipidémie liée à l’obésité, qui est la forme de dyslipidémie secondaire la plus courante, se manifeste généralement par une hypertriglycéridémie légère à modérée et un faible taux de cholestérol à lipoprotéines de haute densité (HDL-C), mais le risque cardiovasculaire sous-jacent est lié au nombre accru de petites particules denses de lipoprotéines de basse densité[6].
Les motifs du dépistage et du traitement précoces
L’athérosclérose se manifeste pendant l’enfance, mais les troubles lipidiques demeurent souvent invisibles sur le plan clinique et peuvent donc facilement passer inaperçus. Par exemple, malgré la forte prévalence d’HF[10][15] et la relative facilité à poser un diagnostic (par bilan lipidique de dépistage), environ 90 % des cas d’HF hétérozygotes demeurent non détectés[9]. La détection et le traitement précoces de l’HF réduisent le fardeau cumulatif du LDL-C (et, par conséquent, celui de l’athérosclérose) et présentent des avantages importants à long terme sur la santé et la situation socioéconomique[9][16]. Malheureusement, les stratégies de dépistage sélectives qui reposent sur l’histoire familiale ratent de 30 % à 60 % des cas de dyslipidémies chez les jeunes[17]. Les directives antérieures recommandaient le dépistage universel par bilan lipidique non à jeun de tous les enfants de neuf à 11 ans, et une reprise du dépistage entre l’âge de 17 et 21 ans pour améliorer la détection de l’HF et des autres troubles lipidiques héréditaires[7].
De nombreuses études observationnelles randomisées et prospectives ont démontré qu’un traitement aux statines chez les enfants atteints d’HF réduit bel et bien leur LDL-C et peut ralentir considérablement, sinon normaliser, l’évolution de l’athérosclérose et la MCV[18]-[22]. Les motifs et les données probantes en appui à un dépistage précoce et à l’amorce rapide d’un traitement aux statines chez les enfants atteints d’HF sont convaincantes. Il est à souligner que les données en appui au traitement précoce d’autres phénotypes des dyslipidémies le sont moins en pédiatrie.
Les stratégies de dépistage
Le recours à un panneau lipidique pour détecter la dyslipidémie est simple et facile à inclure dans les soins primaires réguliers. Deux stratégies sont utilisées dans la pratique : 1) le dépistage sélectif ou universel et 2) le dépistage en cascade ou à rebours en cascade.
Le dépistage sélectif ou universel
Le dépistage sélectif des lipides est indiqué chez les enfants de plus de deux ans qui possèdent une histoire familiale de MCV prématurée (angine, infarctus du myocarde, coronaropathie ou décès cardiaque soudain chez un parent, un grand-parent, une tante ou un oncle de moins de 55 ans chez les hommes et de moins de 65 ans chez les femmes)[7]. Il s’applique aussi aux enfants atteints de certaines affections (p. ex., diabète de type 2, néphropathie chronique) ou qui présentent des facteurs de risque de MCV prématurée (p. ex., obésité, hypertension, tabagisme)[7][23]. Malheureusement, le dépistage sélectif ne convient pas à la détection de l’HF. Une stratégie de dépistage universelle est recommandée, dans un groupe un peu plus jeune que la population des neuf à 11 ans[7][24], car elle est plus pratique dans le contexte canadien pour détecter l’HF et qu’elle prévient mieux la dyslipidémie permanente. Le dépistage devrait toutefois se produire après l’âge de deux ans, puisque les taux de LDL-C se chevauchent considérablement entre les cas d’HF confirmés sur le plan moléculaire et l’absence de cas chez les enfants de moins de deux ans[25].
Le dépistage en cascade ou à rebours en cascade
Le dépistage familial en cascade des parents au premier degré des personnes atteintes d’HF[26], y compris le dépistage génétique lorsqu’il est disponible, vise à détecter les mutations génétiques particulières qui influent plus ou moins sur la présence et la gravité de la dyslipidémie[9][27]. L’intégration du dépistage de l’HF aux soins primaires faciliterait non seulement la détection de l’HF chez les enfants plus jeunes, mais également chez les parents (grâce au dépistage à rebours en cascade, accompagné ou non de dépistage génétique) bien avant l’apparition d’une MCV[28]. Cette stratégie s’est révélée efficiente au Royaume-Uni[29]. Une évaluation plus approfondie s’impose en contexte canadien.
Les bilans lipidiques à jeun ou non à jeun
La mesure des taux de cholestérol non à lipoprotéines de haute densité non à jeun (cholestérol total déduction faite du HDL-C) constituent un test de dépistage simple et approprié qui prédit très bien la présence et la persistance de la dyslipidémie, parce qu’elle fournit les taux d’apolipoprotéine B[7]. Parmi les paramètres des lipoprotéines, ce sont les taux de triglycérides qui varient le plus selon l’état de jeûne. Lorsqu’on détecte une dyslipidémie lors du dépistage initial chez les patients, le test subséquent devrait se composer d’évaluations à jeun, tel qu’il est exposé ci-dessous.
L’évaluation clinique des dyslipidémies en pédiatrie
L’évaluation des étiologies primaires et secondaires possibles fait partie de l’évaluation clinique des enfants et des adolescents atteints de dyslipidémie. Les dyslipidémies génétiques primaires sont résumées au tableau 3, et certains facteurs contributifs et causes secondaires, au tableau 4 de la mise à jour originale des pratiques cliniques, en anglais. Pour établir la présence d’autres facteurs de risque ou d’autres affections (voir le tableau 2), il faut procéder à une histoire et un examen physique détaillés[6][7][23]. Il est essentiel de catégoriser les affections à risque de MCV prématurée pour orienter les décisions thérapeutiques[30].
L’examen physique devrait inclure la mesure de la taille, du poids et de l’indice de masse corporelle sur des courbes de croissance standardisées, la mesure de la tension artérielle, l’évaluation du stade pubertaire, l’exclusion d’un goitre ou d’une hépatosplénomégalie et la recherche de signes d’insulinorésistance (p. ex., acanthosis nigricans, qui devrait entraîner une évaluation plus détaillée de l’insulinorésistance, du syndrome métabolique ou de ces deux affections). Les observations physiques de dyslipidémie (p. ex., arc cornéen, xanthélasmas ou xanthomes tendineux) laissent toutes croire à une HF homozygote et sont plus rares chez les enfants atteints d’une HF hétérozygote ou d’autres formes de dyslipidémie[31]. Une lipémie rétinienne et des xanthomes éruptifs sur les surfaces des extenseurs et des fesses laissent supposer une hypertriglycéridémie marquée[31], tandis que des antécédents de douleurs abdominales récurrentes évocatrices d’une pancréatite peuvent être indicateurs d’une grave hypertriglycéridémie[32].
L’examen biochimique initial devrait inclure un hémogramme, un bilan lipidique à jeun, le bilan de la thyréostimuline (ou thyréotropine) et de la fonction hépatique et rénale, l’analyse des urines, la glycémie à jeun, l’hémoglobine glyquée et d’autres tests découlant de l’évaluation clinique. En présence d’une dyslipidémie, les décisions relatives au diagnostic et à la pharmacothérapie devraient reposer sur la moyenne des résultats d’au moins deux bilans lipidiques à jeun obtenus à au moins deux semaines (mais pas plus de trois mois) d’écart. En pédiatrie, la détermination des taux de lipoprotéine (a) peut éclairer l’évaluation du risque cardiovasculaire encore davantage, mais la disponibilité du test, la variabilité des dosages et l’absence de standardisation demeurent préoccupantes[13][33][34]. Devant des soupçons de dyslipidémie monogénique (comme l’HF) soulevés par le profil du panneau lipidique (p. ex., LDL-C supérieur à 4,0 mmol/L), le prestataire de soins peut envisager des tests génétiques après avoir exclu les causes secondaires possibles de dyslipidémie. Ce sont généralement des spécialistes des lipides ou de la génétique médicale en pédiatrie qui procèdent aux tests génétiques, mais ils ne sont pas toujours disponibles.
Une démarche de prise en charge de la dyslipidémie
Les conseils sur le régime alimentaire et le mode de vie
D’importantes recommandations nutritionnelles sont préconisées auprès de tous les enfants et adolescents atteints de dyslipidémie : 1) le maintien d’un régime alimentaire sain par rapport à l’âge, conformément au Guide alimentaire canadien, c’est-à-dire riche en légumes, en fruits entiers, en légumineuses, en poissons, en noix, en huiles végétales, en grains entiers, en lait et en yogourt; 2) la consommation plus fréquente de sources de protéines végétales (p. ex., le tofu); 3) l’évitement des gras trans; 4) la baisse de la consommation de gras saturés et 5) la consommation limitée d’aliments ultratransformés. Il est fortement recommandé de consulter en nutrition, mais il est souvent difficile d’avoir accès à ces services. Il est également essentiel d’encourager le respect des Directives canadiennes en matière de mouvement pour les enfants et les adolescents[35] et de préconiser l’abandon du tabac[36].
La diminution du cholestérol à lipoprotéines de basse densité
L’approche nutritionnelle est graduelle en cas de LDL-C élevé[7][37]. Par exemple, en plus d’adhérer aux recommandations du Guide alimentaire canadien et d’adopter un régime méditerranéen, les calories totales tirées des matières grasses devraient être limitées à moins de 30 % (mais pas à moins de 20 %) et les gras saturés, à 8 % à 10 % de l’apport calorique quotidien[7]. Si les taux élevés de LDL-C persistent, il est recommandé de réduire les gras saturés à moins de 7 % et les gras mono-insaturés à moins de 10 % des calories quotidiennes totales.
Les phytostérols (stérols et stanols) sont des composés bioactifs contenus dans des légumes comme le brocoli, les oignons rouges et les carottes. Il est démontré que l’ingestion de 2 g/jour de phytostérols (généralement associée à la prise de suppléments) réduit le LDL-C de 8 % à 10 %[38], même chez les personnes qui suivent un traitement aux statines[39]. Chez ces mêmes personnes, des suppléments de psyllium, une fibre soluble, peuvent réduire le LDL-C d’encore 5 % à 10 % selon la dose[40]. Chez les enfants atteints d’hypercholestérolémie, on peut envisager l’intégration de stérols végétaux (2 g par jour) et de fibres de psyllium (de 6 g/jour chez les deux à 12 ans et de 12 g/jour chez les plus de 12 ans)[7]. Les phytostérols nutritionnels et les suppléments de fibres sont efficaces pour réduire le LDL-C, mais on n’en connaît pas les répercussions sur le risque de MCV.
Les triglycérides
Les enfants et les adolescents qui présentent des taux modérément élevés de triglycérides répondent aux modifications au mode de vie, y compris un régime faible en sucres et en glucides raffinés (pour leur préférer les glucides complexes), faible en matières grasses et riche en fibres[7][41]. On peut également envisager d’accroître la consommation d’aliments riches en acides gras oméga-3[42]. L’activité physique régulière est recommandée, et les causes secondaires des taux élevés de triglycérides, comme l’obésité ou un diabète non contrôlé, doivent être corrigées. Il faut encourager la participation à un programme multidisciplinaire de prise en charge de l’obésité lorsque la situation l’indique. Il est important de restreindre considérablement les matières grasses chez les enfants et les adolescents qui présentent une carence en lipoprotéines lipases et une grave hypertriglycéridémie (supérieure à 10 mmol/L) pour prévenir la pancréatite[41].
La pharmacothérapie
Avant d’envisager la pharmacothérapie de la dyslipidémie, il faut d’abord tenter de modifier l’alimentation et le mode de vie pendant une période raisonnable (généralement six mois, mais cette étape peut être abrégée en cas de dyslipidémie grave [LDL-C de 4,9 mmol/L ou plus]). En pédiatrie, la médication est réservée aux enfants atteints d’une dyslipidémie persistante marquée, d’autres affections à risque ou d’autres facteurs de risque, notamment l’HF (voir le tableau 2). Lorsque la situation l’indique, la pharmacothérapie devrait être associée à une prise en charge du mode de vie.
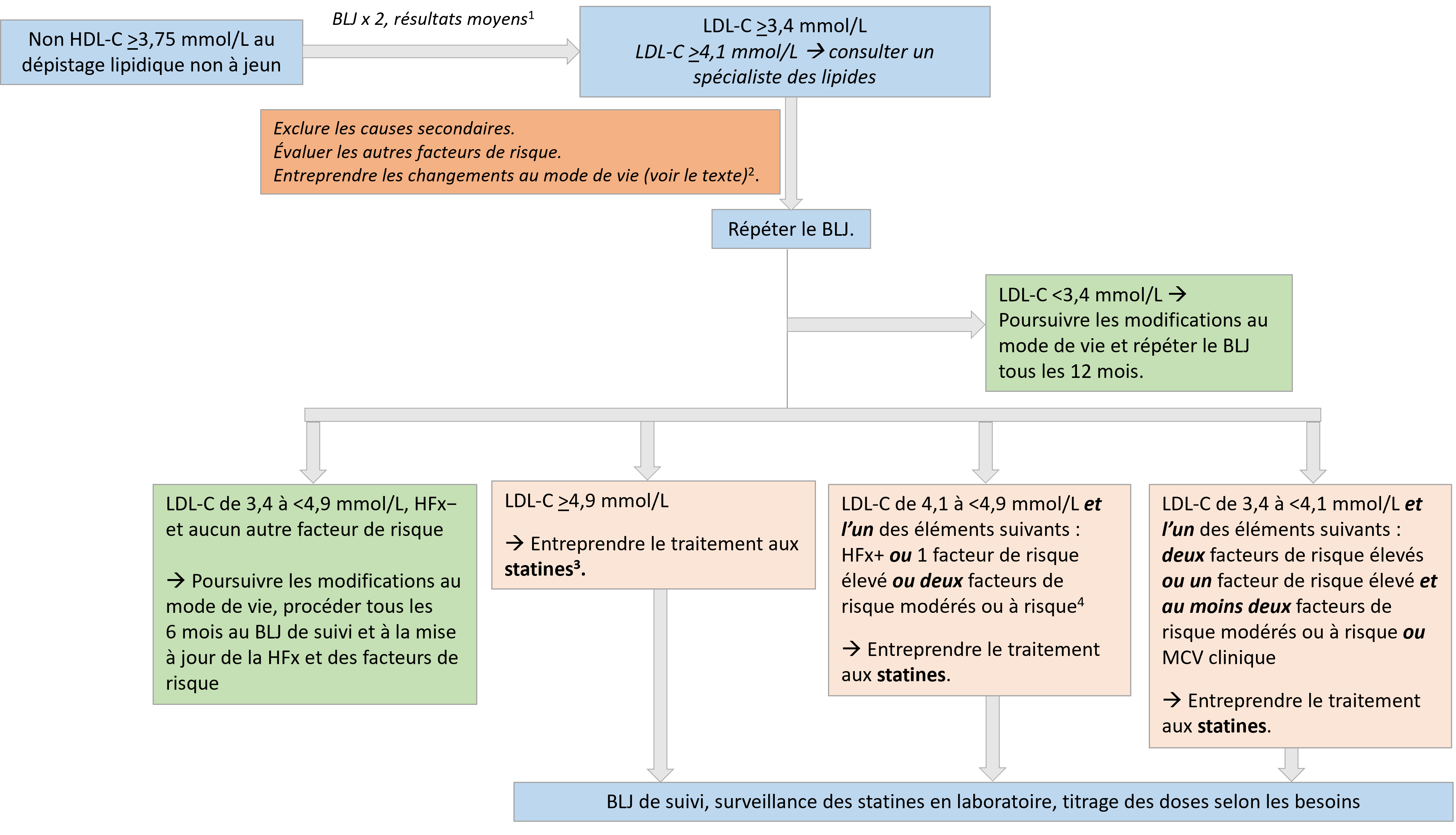
Pour prendre en charge le LDL-C (surtout en présence d’HF), les statines sont les médicaments de première ligne, souvent amorcées lorsque les enfants sont âgés de huit à 12 ans[5][43]. Les recommandations sont énoncées à la figure 1, y compris les seuils pour entreprendre le traitement en fonction des risques sous-jacents. Il est à souligner que les seuils de LDL-C pour entreprendre le traitement aux statines sont plus faibles chez les personnes atteintes de diabète de type 1 ou 2. La surveillance périodique des enzymes hépatiques à des fins de sécurité, de même que celle des symptômes musculaires et d’autres symptômes, les conseils sur la prévention de la grossesse et sur les interactions médicamenteuses et le renforcement de mesures liées au mode de vie sont tous recommandés à la figure 3 de la mise à jour originale des pratiques cliniques, en anglais. Les décisions sur le meilleur moment d’entreprendre la médication doivent être prises conjointement avec la famille, ce qui inclut l’éducation, les conseils préventifs et l’évaluation des préoccupations particulières. La prise en charge pharmacologique des enfants atteints d’HF homozygote doit être lancée dès le diagnostic par un spécialiste des lipides (généralement en cardiologie ou endocrinologie pédiatriques).
Figure 1. Les seuils de statines pour le traitement en pédiatrie
1. Reprendre le BLJ de deux semaines à trois mois après le test de dépistage initial.
2. Envisager d’administrer des suppléments nutritionnels (phytostérols et psyllium).
3. D’ordinaire, les statines sont amorcées entre l’âge de huit et 12 ans. Il est à souligner que dans la population pédiatrique, les seuils de traitement aux statines reposent largement sur des avis d’experts.
4. Voir le tableau 2 pour connaître les affections et les facteurs de risque élevés, de risque modérés et à risque.
BLJ bilan lipidique à jeun; non HDL-C cholestérol non à lipoprotéines de haute densité; LDL-C cholestérol à lipoprotéines de basse densité; HFx− ou HFx+ histoire familiale négative ou positive; IMC indice de masse corporelle; MCV maladie cardiovasculaire
Source : Cette figure a été publiée en anglais par le Journal canadien de cardiologie 38(8), Khoury M, Bigras JL, Cummings EA et coll. The detection, evaluation, and management of dyslipidemia in children and adolescents: A Canadian Cardiovascular Society/Canadian Pediatric Cardiology Association clinical practice update:1168-79. © Elsevier 2022. Traduction autorisée.
Les statines présentent des profils d’innocuité à court et à moyen terme semblables à ceux des adultes chez les enfants de huit ans et plus[18], et les données d’innocuité publiées en 2019 dans une étude de suivi sur 20 ans étaient rassurantes[22]. L’analyse Cochrane la plus récente sur la prise de statines chez les enfants atteints d’HF a démontré qu’il y avait peu de différences, sinon aucunes, entre le traitement et un placebo pour ce qui est de la fonction hépatique, de la créatinine kinase, de la myopathie, des taux d’hormones sexuelles, du stade pubertaire ou des événements cliniques indésirables[18]. Jusqu’à présent, aucune étude clinique n’a révélé de rhabdomyolyse (dégénérescence des muscles squelettiques) attribuable à un traitement aux statines chez les enfants et les adolescents[7]. Néanmoins, tant la prise de statines chez les enfants de moins de huit ans que leur innocuité à long terme chez tous les enfants doivent faire l’objet d’une étude longitudinale. Les risques d’insulinorésistance ou de diabète de type 2 causés par la prise de statines ont davantage suscité l’intérêt ces dernières années. Chez les adultes, les données d’une méta-analyse ont établi que le traitement aux statines de 255 adultes pendant quatre ans entraînerait un cas de diabète de type 2[44]. Le risque de diabète de novo dans la population pédiatrique qui suit un traitement aux statines doit faire l’objet d’études plus approfondies, mais la même étude de suivi sur 20 ans dont il est question plus haut a révélé qu’une personne sur 184 atteinte d’une HF hétérozygote prenant un traitement aux statines a contracté un diabète de type 2, par rapport à deux des 77 membres de la fratrie non touchés[22], ce qui représente des données préliminaires rassurantes au sujet de l’apparition du diabète chez les enfants qui prennent des statines. Il est à souligner que des données émergentes tirées d’une étude clinique pourraient bientôt démontrer l’intérêt d’utiliser de nouveaux médicaments pour abaisser le taux de lipides, y compris des agents biologiques qui ciblent la proprotéine convertase subtilisine/kexine de type 9 (PCSK9)[45][46] indépendamment du récepteur des lipoprotéines de basse densité dans la population pédiatrique[47], élargissant ainsi les options thérapeutiques pour les patients présentant un LDL-C très élevé à cause de dyslipidémies génétiques.
Chez les personnes atteintes d’hypertriglycéridémie, les suppléments nutritionnels d’acides gras oméga-3 peuvent comporter des avantages. Chez les adultes, des doses pharmacologiques de 2 g à 4 g d’acides gras oméga-3 à longue chaîne par jour réduisaient les taux de triglycérides jusqu’à concurrence de 30 %[41], et l’utilisation d’icosapent éthyle (acide éthyl-eicosapentaénoïque) réduisait les incidents de MCV (également chez les adultes, par rapport à l’huile minérale) dans l’étude REDUCE-IT[48]. Cependant, d’autres formulations d’acides gras oméga-3 sur ordonnance, qui renferment à la fois de l’éthyl-eicosapentaénoïque et de l’acide docosahexaénoïque, ne réduisaient pas les incidents de MCV dans une mesure similaire[49]. Par ailleurs, de petites études randomisées sur le traitement par acides gras oméga-3 chez les enfants et les adolescents n’ont pas démontré d’améliorations statistiquement significatives des taux de triglycérides par rapport à un placebo[50].
Des formulations d’acides gras oméga-3 devraient être prescrites aux enfants et aux adolescents parce que les suppléments en vente libre contiennent souvent des taux moins élevés d’éthyl-eicosapentaénoïque et d’acide docosahexaénoïque, n’ont peut-être pas fait l’objet d’une surveillance règlementaire comparable de leur innocuité et peuvent contenir des contaminants au potentiel nuisible, comme des toxines et des acides gras oxydés[51]. Les personnes allergiques aux poissons ou qui ont des préférences alimentaires particulières devraient consulter leur médecin pour connaître les formulations d’oméga-3 appropriées. D’autres discussions au sujet de la pharmacothérapie de l’hypertriglycéridémie sont incluses dans la mise à jour originale des pratiques cliniques[5]. En général, un traitement pharmacologique de l’hypertriglycéridémie persistante (triglycérides plasmatiques de 2,3 à 5,5 mmol/L malgré des interventions sur le mode de vie) ou grave (plus de 5,5 mmol/L), y compris l’utilisation d’acides gras à oméga-3 ou de fibrates sur ordonnance, peut être envisagé conjointement avec une prise en charge nutritionnelle rigoureuse, même si les données probantes sur les avantages et l’innocuité sont limitées chez les enfants. L’évaluation et la prise en charge par un spécialiste des lipides sont recommandées, notamment lorsqu’on envisage l’administration de fibrates en raison de leurs interactions médicamenteuses importantes et de leur profil d’effets indésirables.
Conclusion
En pédiatrie, les troubles lipidiques, y compris les troubles génétiques comme l’HF qui entraînent une dyslipidémie marquée, sont courants et accroissent le risque de maladie cardiovasculaire prématurée. Le traitement de l’HF dès l’enfance peut normaliser le risque cardiovasculaire. Cette affection passe généralement inaperçue sur le plan clinique et exige une évaluation du bilan lipidique pour qu’il soit possible de poser un diagnostic. Une démarche qui intègre un dépistage universel, en cascade et sélectif constitue la stratégie la plus complète pour détecter les enfants à risque et favoriser un traitement rapide.
Principaux points et recommandations
- L’athérosclérose se manifeste pendant l’enfance. Sa présence et sa gravité sont liées à des facteurs de risque cardiovasculaires, y compris la dyslipidémie.
- L’hypercholestérolémie familiale (HF) est courante (environ un cas sur 300 personnes) et facile à détecter grâce au test de dépistage du cholestérol à lipoprotéines de basse densité (LDL-C), mais demeure très peu diagnostiquée au Canada.
- Le dépistage lipidique universel est recommandé entre l’âge de deux et de dix ans, au moyen du dépistage du cholestérol à lipoprotéines de haute densité, à jeun ou non, ou du LDL-C. Dans les cas d’HF définitive ou probable, ce test devrait être conjugué au dépistage en cascade des membres de la famille pour détecter les autres personnes touchées. Le dépistage sélectif devrait être envisagé en tout temps chez les enfants présentant des facteurs de risque cardiovasculaire connus, des affections qui prédisposent à un risque accru ou une histoire familiale de maladie cardiovasculaire ou de dyslipidémie prématurées.
- Une histoire approfondie et un examen physique s’imposent, en plus d’examens supplémentaires si la situation l’indique, pour exclure les causes secondaires de dyslipidémie chez les enfants.
- La prise en charge du mode de vie et de l’alimentation sont des stratégies thérapeutiques de première ligne dans pratiquement tous les cas de dyslipidémie chez les enfants. Les conseils incluent le respect du Guide alimentaire canadien et des Directives canadiennes en matière de mouvement pour les enfants et les jeunes de la Société canadienne de physiologie de l’exercice.
- Après le début du traitement aux hypolipémiants, la prise en charge du mode de vie et de l’alimentation continue d’être importante.
- Le diagnostic clinique et les décisions communes au sujet de la pharmacothérapie découlent de la moyenne d’au moins deux bilans lipidiques à jeun obtenus à au moins deux semaines (mais pas plus de trois mois) d’écart.
- L’orientation vers un spécialiste des lipides en pédiatrie peut faciliter la prise en charge du mode de vie ou de la pharmacothérapie, particulièrement en cas de dyslipidémie marquée au diagnostic (LDL-C d’au moins 4,1 mmol/L ou taux de triglycérides d’au moins 5,5 mmol/L) ou de dyslipidémie accompagnée de facteurs de risque ou d’affections à risque (voir le tableau 2).
- Un traitement aux statines peut être envisagé entre l’âge de huit et 12 ans si le LDL-C de l’enfant demeure au-dessus des seuils prévus malgré la prise en charge du mode de vie (voir la figure 1). La surveillance régulière de l’innocuité et des cibles thérapeutiques du LDL-C sont des aspects incontournables des soins et de la prise en charge.
Remerciements
Le comité de la santé de l’adolescent et le comité de la gastroentérologie et de la nutrition de la Société canadienne de pédiatrie ont révisé le présent document de principes.
COMITÉ DE LA PÉDIATRIE COMMUNAUTAIRE DE LA SOCIÉTÉ CANADIENNE DE PÉDIATRIE (2023-2024)
Membres : Peter Wong MD (président), Jill Borland Starkes MD (représentante du conseil), Michael Hill MD, Audrey Lafontaine MD, Meta van den Heuvel MD, Kelcie Lahey MD M. Sc.
Représentante : Richa Agnihotri MD (section de la pédiatrie communautaire de la SCP)
Auteurs principaux : Michael Khoury MD, Jean-Luc Bigras MD, Elizabeth A. Cummings MD, Kevin C. Harris MD M Sc. S. , Robert A. Hegele MD, Mélanie Henderson MD Ph. D., Katherine M. Morrison MD, Julie St-Pierre MD Ph. D., Peter D. Wong MD Ph. D., Brian W. McCrindle MD MHP
Financement
Aucun financement n’a été accordé pour la préparation du présent manuscrit.
Conflits d’intérêts potentiels
MK a siégé à des conseils consultatifs d’Ultragenyx.
BWM est consultant pour Amryt Pharma, Chiesi, Esperion et Ultragenyx.
RH déclare avoir reçu des honoraires d’Amgen, de HLS Therapeutics et de Sanofi, est membre des comités consultatifs scientifiques d’Amgen, de HLS Therapeutics, de Novartis, de Pfizer, de Sanofi, d’Acasti, d’Aegerion, d’Akoea et d’Arrowhead et a reçu un financement ou des subventions d’Amgen, d’Arrowhead, de The Medicines Company, de LIB Therapeutics, de Novartis et de Regeneron.
MH déclare avoir reçu des subventions de recherche des Instituts de recherche en santé du Canada, de Diabète Québec, du Fonds de recherche du Québec – Santé et du Réseau de recherche en santé cardiométabolique, diabète et obésité et est membre non rémunérée du comité scientifique sur la prévention de l’obésité et de l’Institut national de santé publique du Québec.
KM est membre des comités consultatifs de Novo Nordisk et de Rhythm Pharmaceuticals, ainsi que du comité de surveillance sur la sécurité des données de Novartis.
JSP déclare avoir reçu des subventions d’éducation sur l’obésité de Novo Nordisk et de Lilly et est membre du comité mondial de prise en charge clinique de Novo Nordisk.
Aucun autre conflit d’intérêts n’a été déclaré.
Références
- Berenson GS, Srinivasan SR, Bao W et coll. Association between multiple cardiovascular risk factors and atherosclerosis in children and young adults. The Bogalusa Heart Study. N Engl J Med 1998;338(23):1650-6. doi : 10.1056/NEJM199806043382302
- McGill HC, McMahan CA, Zieske AW et coll. Associations of coronary heart disease risk factors with the intermediate lesion of atherosclerosis in youth. The Pathobiological Determinants of Atherosclerosis in Youth (PDAY) Research Group. Arterioscler Thromb Vasc Biol 2000;20(8):1998-2004. doi : 10.1161/01.atv.20.8.1998
- Khoury M, Rodday AM, Mackie AS et coll. Pediatric lipid screening and treatment in Canada: Practices, attitudes, and barriers. Can J Cardiol 2020;36(9):1545-9. doi : 10.1016/j.cjca.2020.05.035
- Christian S, Ridsdale R, Lin M, Khoury M. Evaluating the prevalence of lipid assessments in children in Alberta, Canada. CMAJ Open 2023;11(5):E820-5. doi : 10.9778/cmajo.20220163
- Khoury M, Bigras JL, Cummings EA et coll. The detection, evaluation, and management of dyslipidemia in children and adolescents: A Canadian Cardiovascular Society/Canadian Pediatric Cardiology Association clinical practice update. Can J Cardiol 2022;38(8):1168-79. doi : 10.1016/j.cjca.2022.05.002
- Lazarte J, Hegele RA. Pediatric dyslipidemia—Beyond familial hypercholesterolemia. Can J Cardiol 2020;36(9):1362-71. doi : 10.1016/j.cjca.2020.03.020
- Expert Panel on Integrated Guidelines for Cardiovascular Health and Risk Reduction in Children and Adolescents; National Heart, Lung, and Blood Institute. Summary report. Pediatrics 2011;128(Suppl 5):S213-56. doi : 10.1542/peds.2009-2107C
- Hegele RA, Borén J, Ginsberg HN et coll. Rare dyslipidaemias, from phenotype to genotype to management: A European Atherosclerosis Society task force consensus statement. Lancet Diabetes Endocrinol 2020;8(1):50-67. doi : 10.1016/S2213-8587(19)30264-5
- Wiegman A, Gidding SS, Watts GF et coll. Familial hypercholesterolaemia in children and adolescents: Gaining decades of life by optimizing detection and treatment. Eur Heart J 2015;36(36):2425-37. doi : 10.1093/eurheartj/ehv157
- Brunham LR, Ruel I, Aljenedil S et coll. Canadian Cardiovascular Society position statement on familial hypercholesterolemia: Update 2018. Can J Cardiol 2018;34(12):1553-63. doi : 10.1016/j.cjca.2018.09.005
- Ruel I, Brisson D, Aljenedil S et coll. Simplified Canadian definition for familial hypercholesterolemia. Can J Cardiol 2018;34(9):1210-4. doi : 10.1016/j.cjca.2018.05.015
- Dron JS, Hegele RA. Genetics of hypertriglyceridemia. Front Endocrinol (Lausanne) 2020;11:455. doi : 10.3389/fendo.2020.00455
- Tsimikas S. A test in context: Lipoprotein(a); Diagnosis, prognosis, controversies, and emerging therapies. J Am Coll Cardiol 2017;69(6):692-711. doi : 10.1016/j.jacc.2016.11.042
- Raitakari O, Kartiosuo N, Pahkala K et coll. Lipoprotein(a) in youth and prediction of major cardiovascular outcomes in adulthood. Circulation 2023;147(1):23-31. doi : 10.1161/circulationaha.122.060667
- de Ferranti SD, Rodday AM, Mendelson MM et coll. Prevalence of familial hypercholesterolemia in the 1999 to 2012 United States National Health and Nutrition Examination Surveys (NHANES). Circulation 2016;133(11):1067-72. doi : 10.1161/circulationaha.115.018791
- Defesche JC, Gidding SS, Harada-Shiba M et coll. Familial hypercholesterolaemia. Nat Rev Dis Primers 2017;3:17093. doi : 10.1038/nrdp.2017.93
- Haney EM, Huffman LH, Bougatsos C et coll. Screening and treatment for lipid disorders in children and adolescents: Systematic evidence review for the US Preventive Services Task Force. Pediatrics 2007;120(1):e189-214. doi : 10.1542/peds.2006-1801
- Vuorio A, Kuoppala J, Kovanen PT et coll. Statins for children with familial hypercholesterolemia. Cochrane Database Syst Rev 2019;2019(11):CD006401. doi : 10.1002/14651858.CD006401.pub5
- Khoury M, McCrindle BW. The rationale, indications, safety, and use of statins in the pediatric population. Can J Cardiol 2020;36(9):1372-83. doi : 10.1016/j.cjca.2020.03.041
- de Jongh S, Lilien MR, op’t Roodt J et coll. Early statin therapy restores endothelial function in children with familial hypercholesterolemia. J Am Coll Cardiol 2002;40(12):2117-21. doi : 10.1016/s0735-1097(02)02593-7
- Wiegman A, Hutten BA, de Groot E et coll. Efficacy and safety of statin therapy in children with familial hypercholesterolemia: A randomized controlled trial. JAMA 2004;292(3):331-7. doi : 10.1001/jama.292.3.331
- Luirink IK, Wiegman A, Kusters DM et coll. 20-year follow-up of statins in children with familial hypercholesterolemia. N Engl J Med 2019;381(16):1547-56. doi : 10.1056/NEJMoa1816454
- Khoury M, Kavey REW, St Pierre J, McCrindle BW. Incorporating risk stratification into the practice of pediatric preventive cardiology. Can J Cardiol 2020;36(9):1417-28. doi : 10.1016/j.cjca.2020.06.025
- Goldberg AC, Hopkins PN, Toth PP et coll. Familial hypercholesterolemia: Screening, diagnosis and management of pediatric and adult patients; Clinical guidance from the National Lipid Association Expert Panel on Familial Hypercholesterolemia. J Clin Lipidol 2011;5(3):133-40. doi : 10.1016/j.jacl.2011.03.001
- Vuorio AF, Turtola H, Kontula K. Neonatal diagnosis of familial hypercholesterolemia in newborns born to a parent with a molecularly defined heterozygous familial hypercholesterolemia. Arterioscler Thromb Vasc Biol 1997;17(11):3332-7. doi : 10.1161/01.atv.17.11.3332
- Wald DS, Bestwick JP. Reaching detection targets in familial hypercholesterolaemia: Comparison of identification strategies. Atherosclerosis 2020;293:57-61. doi : 10.1016/j.atherosclerosis.2019.11.028
- Brown EE, Sturm AC, Cuchel M et coll. Genetic testing in dyslipidemia: A scientific statement from the National Lipid Association. J Clin Lipidol 2020;14(4):398-413. doi : 10.1016/j.jacl.2020.04.011
- Wald DS, Bestwick JP, Morris JK et coll. Child-parent familial hypercholesterolemia screening in primary care. N Engl J Med 2016;375(17):1628-37. doi : 10.1056/NEJMoa1602777
- McKay AJ, Hogan H, Humphries SE et coll. Universal screening at age 1-2 years as an adjunct to cascade testing for familial hypercholesterolaemia in the UK: A cost-utility analysis. Atherosclerosis 2018;275:434-43. doi : 10.1016/j.atherosclerosis.2018.05.047
- de Ferranti SD, Steinberger J, Ameduri R et coll. Cardiovascular risk reduction in high-risk pediatric patients: A scientific statement from the American Heart Association. Circulation 2019;139(13):e603-34. doi : 10.1161/CIR.0000000000000618
- Descamps OS, Tenoutasse S, Stephenne X et coll. Management of familial hypercholesterolemia in children and young adults: Consensus paper developed by a panel of lipidologists, cardiologists, paediatricians, nutritionists, gastroenterologists, general practitioners and a patient organization. Atherosclerosis 2011;218(2):272-80. doi : 10.1016/j.atherosclerosis.2011.06.016
- Shah AS, Wilson DP. Primary hypertriglyceridemia in children and adolescents. J Clin Lipidol 2015;9(5 Suppl):S20-8. doi : 10.1016/j.jacl.2015.04.004
- Alonso R, Andres E, Mata N et coll. Lipoprotein(a) levels in familial hypercholesterolemia: An important predictor of cardiovascular disease independent of the type of LDL receptor mutation. J Am Coll Cardiol 2014;63(19):1982-9. doi : 10.1016/j.jacc.2014.01.063
- Ellis KL, Pérez de Isla L, Alonso R et coll. Value of measuring lipoprotein(a) during cascade testing for familial hypercholesterolemia. J Am Coll Cardiol 2019;73(9):1029-39. doi : 10.1016/j.jacc.2018.12.037
- Société canadienne de physiologie de l’exercice. Directives canadiennes en matière de mouvement sur 24 heures pour les enfants et les jeunes (5 à 17 ans) : Une approche intégrée regroupant l’activité physique, le comportement sédentaire et le sommeil (consulté le 3 octobre 2025).
- Harvey J, Chadi N. Des stratégies pour promouvoir l’abandon du tabac chez les adolescents. Paediatr Child Health 2016;21(4):205-8. doi : 10.1093/pch/21.4.205
- Grundy SM, Stone NJ, Bailey AL et coll. 2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/APhA/ ASPC/NLA/PCNA Guideline on the management of blood cholesterol: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation 2019;139(25):e1082-143. doi : 10.1161/CIR.0000000000000625
- Katan MB, Grundy SM, Jones P et coll.; participants à l’atelier Stresa. Efficacy and safety of plant stanols and sterols in the management of blood cholesterol levels. Mayo Clin Proc 2003;78(8):965-78. doi : 10.4065/78.8.965
- Han S, Jiao J, Xu J et coll. Effects of plant stanol or sterol-enriched diets on lipid profiles in patients treated with statins: Systematic review and meta-analysis. Sci Rep 2016;6:31337. doi : 10.1038/srep31337
- Brum J, Ramsey D, McRorie J et coll. Meta-analysis of usefulness of psyllium fiber as adjuvant antilipid therapy to enhance cholesterol lowering efficacy of statins. Am J Cardiol 2018;122(7):1169-74. doi : 10.1016/j.amjcard.2018.06.040
- Mach F, Baigent C, Catapano AL et coll. 2019 ESC/EAS guidelines for the management of dyslipidaemias: Lipid modification to reduce cardiovascular risk. Eur Heart J 2020;41(1):111-88. doi : 10.1093/eurheartj/ehz455
- Abdelhamid AS, Brown TJ, Brainard JS et coll. Omega-3 fatty acids for the primary and secondary prevention of cardiovascular disease. Cochrane Database Syst Rev 2020;3(3):CD003177. doi : 10.1002/14651858.CD003177.pub5
- Rodenburg J, Vissers MN, Wiegman A et coll. Statin treatment in children with familial hypercholesterolemia: The younger, the better. Circulation 2007;116(6):664-8. doi : 10.1161/CirculationAHA.106.671016
- Sattar N, Preiss D, Murray HM et coll. Statins and risk of incident diabetes: A collaborative meta-analysis of randomised statin trials. Lancet 2010;375(9716):735-42. doi : 10.1016/S0140-6736(09)61965-6
- Santos RD, Ruzza A, Hovingh GK et coll. Evolocumab in pediatric heterozygous familial hypercholesterolemia. N Engl J Med 2020;383(14):1317-27. doi : 10.1056/NEJMoa2019910
- Daniels S, Caprio S, Chaudhari U et coll. PCSK9 inhibition with alirocumab in pediatric patients with heterozygous familial hypercholesterolemia: The ODYSSEY KIDS study. J Clin Lipidol 2020;14(3):322-30.e5. doi : 10.1016/j.jacl.2020.03.001
- Wiegman A, Greber-Platzer S, Ali S et coll. Evinacumab for pediatric patients with homozygous familial hypercholesterolemia. Circulation 2024;149(5):343-53. doi : 10.1161/CirculationAHA.123.065529
- Bhatt DL, Steg PG, Miller M et coll. Cardiovascular risk reduction with icosapent ethyl for hypertriglyceridemia. N Engl J Med 2019;380(1):11-22. doi : 10.1056/NEJMoa1812792
- Nicholls SJ, Lincoff AM, Garcia M et coll. Effect of high-dose omega-3 fatty acids vs corn oil on major adverse cardiovascular events in patients at high cardiovascular risk: The STRENGTH randomized clinical trial. JAMA 2020;324(22):2268-80. doi : 10.1001/jama.2020.22258
- de Ferranti SD, Milliren CE, Denhoff ER et coll. Using high-dose omega-3 fatty acid supplements to lower triglyceride levels in 10- to 19-year-olds. Clin Pediatr (Phila) 2014;53(5):428-38. doi : 10.1177/0009922814528032
- Fialkow J. Omega-3 fatty acid formulations in cardiovascular disease: Dietary supplements are not substitutes for prescription products. Am J Cardiovasc Drugs 2016;16(4):229-39. doi : 10.1007/s40256-016-0170-7
Avertissement : Les recommandations du présent document de principes ne constituent pas une démarche ou un mode de traitement exclusif. Des variations tenant compte de la situation du patient peuvent se révéler pertinentes. Les adresses Internet sont à jour au moment de la publication.