Document de principes
La prémédication en vue de la laryngoscopie chez les nouveau-nés
Affichage : le 20 avril 2026
Auteur(s) principal(aux)
Anne-Sophie Gervais MD, Keith J. Barrington MD, Emer Finan MB, Société canadienne de pédiatrie, Comité d’étude du fœtus et du nouveau-né
Résumé
La laryngoscopie, courante en soins intensifs néonatals, a des effets indésirables confirmés. Il est démontré que la prémédication réduit ces effets et accroît le taux de réussite. Dans toutes les intubations non urgentes, il faut administrer une prémédication composée d’un vagolytique, d’un opioïde à action rapide et d’un relaxant musculaire à courte durée d’action. Des mesures non pharmacologiques sont toutefois toujours à privilégier en cas d’administration non invasive de surfactant. Les opioïdes à action rapide sont également recommandés, en combinaison avec un vagolytique. La laryngoscopie doit toujours être exécutée ou supervisée par un prestataire de soins qualifié, conjuguée à une surveillance cardiorespiratoire continue.
Mots-clés : administration moins invasive de surfactant; administration de surfactant; laryngoscopie; nouveau-né; prémédication; traitement mini-invasif au surfactant
La laryngoscopie, l’une des interventions les plus utilisées en soins intensifs néonatals, est reconnue pour être une expérience douloureuse et stressante[1][2]. Depuis de nombreuses années, la prémédication en vue de la laryngoscopie augmente, mais les variations sont importantes dans la pratique[3][4]. Les techniques récentes d’administration moins invasive de surfactant ou de traitement mini-invasif au surfactant (LISA ou MIST, d’après les termes anglais)[5] exigent également une laryngoscopie. Aucun consensus ne s’est dégagé à l’égard de la prémédication[6]-[9] et des médicaments à privilégier pour procéder à ces techniques récentes d’administration de surfactant.
On reconnaît de plus en plus les effets de la douleur et du stress non traités chez les nouveau-nés, de même que les données probantes croissantes qui démontrent les effets indésirables d’une exposition répétée à la douleur et au stress[1][10]-[12] et leurs conséquences neurodéveloppementales à long terme sur le cerveau en développement[13]. Les médecins et les autres soignants ont également le devoir éthique de limiter la douleur et de recourir à l’analgésie lors d’interventions douloureuses non urgentes.
Le présent document de principes remplace celui que la Société canadienne de pédiatrie a publié en 2011[14] et fournit des recommandations sur la prémédication en vue d’une laryngoscopie et de l’utilisation des techniques plus récentes d’administration de surfactant.
Quelles sont les réponses physiologiques à la laryngoscopie?
La plupart des recherches portent sur les réponses physiologiques à la laryngoscopie en vue d’une intubation endotrachéale, mais la laryngoscopie peut avoir des répercussions importantes, même avant l’introduction de la sonde endotrachéale. Les réponses physiologiques à la laryngoscopie chez les nouveau-nés éveillés incluent des modifications à la fréquence cardiaque, à la tension artérielle, à la saturation en oxygène et à la pression intracrânienne[15]. Un nouveau-né dont la sédation est insuffisante et qui résiste à l’intervention peut présenter une augmentation de la pression thoracique accompagnée d’une diminution du retour veineux, laquelle est responsable d’une hypertension intracrânienne susceptible d’entraîner une hémorragie intraventriculaire[16] et une leucomalacie périventriculaire[17][18]. Les hausses de la pression intracrânienne peuvent également être attribuables à l’hypoxie ou à l’hypercapnie et à l’extension du cou, qui provoquent une obstruction veineuse[19]. Ces effets peuvent tous être prévenus par des relaxants neuromusculaires, qui réduisent ou éliminent les réponses d’accroissement de la pression intracrânienne[20]. La laryngoscopie et l’intubation endotrachéale provoquent une hausse marquée de la pression artérielle, qui peut souvent dépasser plus de 60 % de la tension artérielle moyenne[17][20]. Selon toute probabilité, l’hypoxémie est partiellement causée par l’apnée, qui peut découler de la stimulation vagale. De plus, le pharynx et les voies respiratoires supérieures peuvent être déformés pendant la laryngoscopie et provoquer une obstruction respiratoire qui contribue encore davantage à l’hypoxémie[21]. La laryngoscopie entraîne souvent un ralentissement de la fréquence cardiaque, probablement à cause de la stimulation vagale et des tentatives prolongées pour réussir l’intervention, lesquelles sont responsables d’une hypoxémie[22].
Une prémédication devrait-elle être utilisée avant la laryngoscopie?
La prémédication par divers médicaments (vagolytiques, analgésiques, sédatifs, relaxants musculaires) a des effets bénéfiques, y compris une meilleure réussite de l’intervention, la durée plus courte des tentatives, une diminution de la douleur et du stress et une baisse des effets physiologiques indésirables[1][2][15][23]-[26]. Il est crucial de limiter à la fois le nombre de tentatives et la durée de chacune d’elles pour réduire les perturbations physiologiques qui y sont associées[21]. Une autre étape essentielle pour optimiser l’état physiologique consiste à stabiliser le nouveau-né avant l’intervention, y compris une oxygénation suffisante qui limite le risque de détérioration pendant l’intervention. Il est particulièrement important de viser une assistance respiratoire optimale et des saturations normales avant l’intervention[27].
Quels médicaments devraient être utilisés avant une laryngoscopie?
À moins d’une raison importante d’éviter la médication, une analgésie appropriée doit être administrée aux nouveau-nés avant les tentatives de laryngoscopie non urgente[2][13][28]. L’ajout d’un anticholinergique (atropine ou glycopyrrolate) est également efficace pour éviter la bradycardie[29][30]. Les caractéristiques de divers médicaments dont l’utilisation a fait l’objet d’études dans le cadre de l’intubation néonatale sont exposées ci-dessous.
Les opioïdes
Les opioïdes sont souvent utilisés pour gérer la douleur néonatale ainsi que pour assurer une analgésie et divers degrés de sédation. La morphine a fait l’objet d’études approfondies dans de tels contextes, mais n’est pas efficace pour réduire l’instabilité physiologique (p. ex., hypoxie, bradycardie, hypertension systémique) ou la durée de l’intubation, probablement en raison de son délai avant d’agir[17]. Le fentanyl, qui commence à agir plus rapidement (au bout de deux à trois minutes), est plus efficace que la morphine pour réduire la douleur et l’instabilité. Le rémifentanil agit rapidement lui aussi et a l’avantage supplémentaire d’avoir une clairance rapide[24]. Cependant, le fentanyl et le rémifentanil comportent tous deux un risque de rigidité de la paroi thoracique[16] et peuvent également provoquer une hypoventilation. Ils doivent être injectés par voie intraveineuse (IV), lentement (sur deux à cinq minutes), incluant la première partie du rinçage, et l’équipe soignante doit être prête à fournir une ventilation assistée en cas d’apnée, d’hypoventilation ou de rigidité de la paroi thoracique. Les relaxants musculaires peuvent renverser la rigidité de la paroi thoracique[22][31]. Le fentanyl par voie intranasale (IN) est également utilisé pour un éventail d’interventions chez les nouveau-nés, y compris l’intubation[32]-[34], mais son délai d’action est long, et son utilisation doit être limitée à des scénarios où l’accès veineux n’est pas praticable.
Le propofol
Le propofol est un anesthésique général largement utilisé pour l’intubation des adultes. Une étude randomisée auprès de 63 nouveau-nés, qui comparait le propofol à une association de morphine, d’atropine et de succinylcholine pour l’intubation, a démontré que les nouveau-nés qui recevaient du propofol étaient intubés deux fois plus vite que le groupe qui recevait de la morphine, de l’atropine et de la succinylcholine, sans entraîner de différence importante de leur fréquence cardiaque et de leur tension artérielle[35]. Une autre comparaison du propofol et de l’atropine à une association d’atracurium, de sufentanil et d’atropine a démontré une meilleure sédation et une intubation plus rapide dans le groupe du sufentanil[36]. Par ailleurs, il est démontré que le propofol provoque une hypotension, particulièrement aux taux élevés nécessaires pour parvenir à une sédation appropriée. C’est pourquoi il est peu utilisé chez les nouveau-nés[37]-[39].
Les benzodiazépines
Les benzodiazépines administrées avant une intervention procurent à la fois une sédation et une amnésie, mais n’ont pas d’effet analgésique. Ils ne devraient donc pas être utilisés seuls, et aucunes données d’étude fiables ne démontrent d’avantage clinique à ajouter du midazolam à un analgésique. Le midazolam, qui est la benzodiazépine la plus utilisée, est souvent combiné à un opioïde[15]. Il agit rapidement et peut également être administré IN (son délai d’action est alors beaucoup plus long) lorsqu’il est impossible d’obtenir un accès IV chez le nouveau-né[15][16]. Son effet hypotensif et sa demi-vie longue et variable peuvent retarder la reprise de la respiration spontanée[40]. Il est également associé à un plus fort taux d’événements indésirables, particulièrement sous forme de sédatif à long terme ou chez des nouveau-nés plus prématurés[41][42].
La kétamine
Les données probantes sur l’administration de kétamine pour intuber les nouveau-nés sont rares. Jusqu’à présent, la seule étude randomisée et contrôlée chez les nouveau-nés (n=60) a comparé la kétamine IN au midazolam IN et révélé que la sédation produite par la kétamine était moins efficace que celle découlant du midazolam. Les deux médicaments avaient des effets hémodynamiques et respiratoires similaires[43].
Les anticholinergiques et les vagolytiques
L’atropine est un anticholinergique utilisé pour prévenir la bradycardie réflexe attribuable à la réponse vagale accrue pendant la laryngoscopie et l’intubation[16]. L’atropine peut également réduire les sécrétions avant cette intervention[44]. Le glycopyrrolate est un analogue de l’atropine qui ne traverse pas la barrière hématoencéphalique et dont la capacité à prévenir la bradycardie pendant l’intubation est démontrée[45].
Les relaxants musculaires
La succinylcholine est un relaxant musculaire dépolarisant à action très rapide (une minute), mais de courte durée (dix minutes). La bradycardie fait partie de ses effets indésirables, et on peut l’éviter par l’administration préalable d’atropine[16]. La succinylcholine comporte également un risque accru d’hyperkaliémie et peut déclencher une hyperthermie maligne[2]. Elle ne devrait donc pas être utilisée chez les nouveau-nés atteints d’hyperkaliémie ou qui ont une histoire familiale d’hyperthermie maligne. Elle est également à éviter chez les enfants ayant un trouble neuromusculaire. Il est établi que la succinylcholine supprime la rigidité de la paroi thoracique causée par l’administration d’opioïdes.
Le rocuronium, le pancuronium et l’atracurium sont des relaxants musculaires non dépolarisants. Le rocuronium agit rapidement (en une à trois minutes), mais a une durée d’action plus longue et variable (jusqu’à une heure), qui le rend moins approprié que la succinylcholine pour l’intubation[14][15]. Le pancuronium est le premier relaxant musculaire à avoir été étudié pour l’intubation, mais il n’est plus disponible en raison du risque de tachycardie auquel il est associé. Sa durée d’action prolongée représentait également un effet négatif. L’atracurium a été étudié au sein d’une association de prémédicaments dans le cadre d’une seule étude randomisée et contrôlée multicentrique (n=173), laquelle a démontré qu’une période médiane de plus de 30 minutes s’écoulait avant le retour au mouvement et à la respiration spontanés, tandis que les nouveau-nés faisant partie du 75e percentile attendaient près d’une heure avant le rétablissement de leur respiration et 65 minutes avant la récupération du mouvement spontané de leurs membres[36].
Quelles sont les complications de la prémédication en vue de l’intubation d’un nouveau-né?
Les effets secondaires à court terme (p. ex., l’instabilité hémodynamique) de la prémédication ont été décrits, de même que la difficulté à en discerner les résultats cliniques à long terme. Certaines études ont démontré une baisse de la tension artérielle sans répercussions connexes sur l’oxygénation cérébrale ou le débit cardiaque[46][47]. Aucunes données probantes ne font état de préjudices importants associés aux effets secondaires d’une prémédication en vue de l’intubation. De même, aucunes données probantes ne démontrent d’effets négatifs de doses occasionnelles d’opioïdes sur l’état neurologique des nouveau-nés[4], mais les données probantes abondent pour confirmer que des interventions répétées et douloureuses sont liées à des résultats cliniques défavorables[2][10]-[12]. De multiples tentatives d’intubation sont également associées à de plus forts taux d’hémorragie intraventriculaire[48]. Grâce à une prémédication appropriée, il est possible de réduire le nombre de tentatives.
Quand est-il acceptable d’intuber un nouveau-né sans prémédication?
La prémédication est recommandée pour toutes les intubations non urgentes. De récentes directives italiennes[2] en faisaient une forte recommandation d’après des données probantes de qualité modérée, tandis qu’une étude française[15] recommandait vivement d’utiliser une prémédication en l’absence de « situations au potentiel mortel immédiat ». Une prépondérance de données probantes appuie l’administration d’une prémédication, à moins qu’un besoin clinique urgent empêche de l’utiliser en toute sécurité (p. ex., en contexte de réanimation néonatale).
Dans les scénarios où il est difficile d’obtenir un accès IV rapidement, il est possible d’administrer du fentanyl IN, dont le délai d’action est de cinq à huit minutes[49]. Il faut toutefois prendre toutes les mesures nécessaires pour prioriser l’accès IV, qui peut être crucial pour la prise en charge des complications. D’autres médicaments IN, comme le midazolam, n’ont pas d’effet analgésique et peuvent provoquer une hypotension[50].
Les nouveau-nés atteints d’anomalies respiratoires ont besoin d’une prémédication individualisée, mais devraient recevoir une analgésie.
Quelles sont les caractéristiques d’un protocole de prémédication acceptable?
Les avantages de l’association d’opioïdes analgésiques à un relaxant musculaire sont bien établis dans les publications scientifiques. Le fentanyl ou le rémifentanil sont favorisés en raison de leur action rapide, mais les utilisateurs doivent connaître la possibilité de rigidité de la paroi thoracique et les signes évocateurs de cet effet secondaire[51]-[53]. Ils doivent également s’assurer d’administrer cet opioïde lentement[25][52].
Des données récentes sur 352 intubations effectuées dans un seul centre ont révélé qu’une « prémédication complète », qui incluait un vagolytique en plus d’un opioïde et d’un relaxant musculaire, était associée à un moins grand nombre d’événements indésirables et à de meilleurs résultats que la « prémédication partielle » à l’aide de ces médicaments ou à l’absence complète de prémédication[26]. Les données de l’étude de cohorte multicentrique Near4Neos portant sur plus de 2 000 intubations ont démontré une baisse des événements indésirables grâce à l’utilisation de relaxants musculaires[25].
Le propofol seul ne peut pas être recommandé pour la plupart des intubations néonatales, car des doses assez élevées pour atténuer les réponses physiologiques provoquent souvent une hypotension[37]-[39]. Le midazolam ne devrait pas être administré seul et n’a pas d’avantages démontrés dans cette situation. L’expérience relative à la kétamine n’est pas suffisante pour en recommander l’utilisation.
D’après les données probantes disponibles, la démarche favorisée pour administrer la prémédication avant l’intubation consisterait à utiliser un vagolytique, un opioïde à action rapide et un relaxant musculaire à courte durée d’action. Les médicaments et les posologies suggérés sont de 0,01 mg/kg à 0,02 mg/kg pour l’atropine, de 2 mcg/kg pour le fentanyl (injectés lentement, sur deux à cinq minutes) et de 2 mg/kg pour la succinylcholine[2] (voir le tableau 1). Le rémifentanil (1 mcg/kg), à action plus rapide, mais plus courte, peut être envisagé en deuxième intention.
Les considérations particulières en fonction des processus pathologiques
Les prestataires de soins devraient connaître les effets secondaires potentiels et les profils pharmacocinétiques des médicaments utilisés. Ils doivent également savoir qu’un dysfonctionnement hépatique et rénal peut affecter la clairance de divers médicaments[2]. L’hypothermie thérapeutique altère l’efficacité de la voie du cytochrome P450, qui réduit l’efficacité de la clairance des opioïdes et du midazolam. Il faudra peut-être opter pour des doses plus faibles de ces deux médicaments[2]. Le rémifentanil se décompose rapidement dans le sang et les tissus et répond moins au dysfonctionnement rénal et hépatique[54].
La prémédication en vue de l’administration de surfactant
Ces dernières années, le recours à l’assistance respiratoire non invasive a augmenté rapidement, conjointement avec l’élaboration de diverses méthodes moins invasives pour administrer les surfactants[8][9]. Lorsqu’une intubation prolongée n’est pas anticipée, la nécessité de maintenir l’activité respiratoire ou de la rétablir rapidement influera sur le choix de la prémédication.
La technique INSURE
Selon la technique INSURE (intubation-surfactant-extubation), le surfactant est administré, puis suivi d’un sevrage et d’une extubation très rapides. Ainsi, les médicaments qui entraînent une dépression respiratoire prolongée sont contre-indiqués. L’administration de médicaments comme la naloxone pour supprimer les effets sédatifs des opioïdes et faciliter une extubation rapide fait également partie des possibilités[55]. Un vagolytique, un opioïde à action rapide (comme le fentanyl ou le rémifentanil) et un relaxant musculaire (comme la succinylcholine) sont recommandés. Les nouveau-nés peuvent toutefois répondre de manière différente aux médicaments; c’est pourquoi il est essentiel d’évaluer l’efficacité respiratoire avant l’extubation[2].
L’administration moins invasive de surfactant ou le traitement mini-invasif au surfactant
De nouvelles techniques d’administration de surfactant, comme le MIST ou la LISA, sont de plus en plus utilisées pour éviter ne serait-ce que de courtes périodes de ventilation mécanique. L’activité respiratoire du nouveau-né doit être maintenue pendant l’une ou l’autre de ces interventions, ce qui a causé une controverse au sujet de la prémédication[6]-[9]. Certains préconisent la prémédication pour tous les nouveau-nés, tandis que d’autres préfèrent une approche personnalisée, qui intègre d’abord des mesures non pharmacologiques, suivies de mesures pharmacologiques au besoin[9]. Un sondage pancanadien publié en 2022 a révélé que dans les 17 centres qui déclaraient utiliser le MIST, la pratique de prémédication était hautement variable : 58,8 % utilisaient de l’atropine, 47 %, du fentanyl, et 35,3 %, de la kétamine[56].
Une récente analyse de deux études randomisées et contrôlées et de quatre études observationnelles a comparé l’utilisation d’une prémédication à l’absence de médicaments chez les nouveau-nés prématurés de 25+6 à 36+6 semaines d’âge gestationnel[57]. Cinq de ces études incluaient peu de sujets, mais une étude de cohorte multicentrique plus vaste[6] comptait 495 nouveau-nés qui avaient fait l’objet de diverses pratiques pharmacothérapeutiques[57]. Une étude randomisée et contrôlée, qui comptait 78 nouveau-nés de 28 à 32 semaines d’âge gestationnel, a comparé le propofol seul à l’absence de prémédication[58]. Cette étude a révélé que le groupe prémédicamenté présentait des scores d’inconfort considérablement plus faibles que le groupe non prémédicamenté[58]. Le groupe prémédicamenté présentait plus de désaturations et avait besoin de plus de ventilation assistée contrôlée intermittente par voie nasale, mais dans l’ensemble, la différence de durée de ce type de ventilation n’était pas significative dans les deux groupes[58]. Une autre petite étude randomisée et contrôlée (n=34; 28+0 à 33+6 semaines d’âge gestationnel), qui comparait le fentanyl à l’absence de prémédication en cas de LISA, a révélé des scores de douleur plus faibles chez les nouveau-nés qui avaient reçu une prémédication[59]. Des désaturations et des besoins en oxygène plus élevés étaient observés chez les nouveau-nés qui recevaient du fentanyl, mais cet effet n’était pas statistiquement significatif[58].
Bien que les données soient encore limitées, une prémédication peut être recommandée lors de toutes les laryngoscopies non urgentes d’après les principes d’une analgésie suffisante pour éviter les répercussions de la douleur à court et à long terme. L’administration de fentanyl ou de rémifentanil est recommandée en cas de LISA ou de MIST, en plus d’un vagolytique comme l’atropine[15][60]. En raison des risques d’apnée et de rigidité de la paroi thoracique, une dose plus faible peut être envisagée (p. ex., 1 mcg/kg de fentanyl), et l’équipe soignante devrait être préparée à effectuer une ventilation en pression positive, à emprunter une autre voie respiratoire ou à procéder à ces deux interventions.
L’administration de surfactant par voie supraglottique
Aucunes données obtenues n’appuient l’utilisation d’une prémédication pour l’administration de surfactant par voie supraglottique. Une analyse a proposé un protocole similaire à celui utilisé pour l’intubation, en fonction de données probantes limitées[15].
|
Médicament |
Posologie |
Voie |
Durée |
Indications |
|
Intubation ou INSURE |
||||
|
Atropine |
De 0,01 mg/kg à 0,02 mg/kg |
IV** |
Injection directe |
Prévention de la bradycardie |
|
Fentanyl |
2 mcg/kg |
IV** |
Injection lente sur 2 à 5 minutes |
Analgésie |
|
Succinylcholine |
2 mg/kg |
IV** |
Injection directe |
Relaxation musculaire |
|
LISA ou MIST |
||||
|
Atropine |
De 0,01 mg/kg à 0,02 mg/kg |
IV** |
Injection directe |
Prévention de la bradycardie |
|
Fentanyl |
1 mcg/kg |
IV** |
Injection lente sur 2 à 5 minutes |
Analgésie |
|
*Lorsqu’il est impossible d’obtenir un accès intraveineux, envisager d’administrer du fentanyl par voie intranasale à une dose de 1 mcg/kg à 2 mcg/kg. Il faut cependant tout mettre en œuvre pour prioriser l’accès intraveineux. **Un bolus rapide de soluté de chlorure de sodium à 9 % est à prévoir pour assurer la clairance du cathéter et de la tubulure, surtout lorsque les volumes administrés sont faibles. INSURE intuber-surfactant-extuber; LISA administration moins invasive de surfactant; MIST traitement mini-invasif au surfactant |
||||
D’autres aspects de l’intubation endotrachéale et de la laryngoscopie
Selon les pratiques exemplaires, toutes les laryngoscopies devraient être effectuées ou supervisées par un prestataire de soins qualifié et expérimenté[14]. La réduction de la durée et du nombre de tentatives atténue le risque de stimulation vagale et d’obstruction respiratoire, qui peuvent entraîner une apnée et une hypoxie[21][27]. L’équipement approprié devrait être installé et le personnel qualifié être en place avant le début de l’intubation et de la laryngoscopie. Les nouveau-nés devraient recevoir l’oxygène nécessaire pour conserver des saturations normales avant l’intervention, et les prestataires devraient être prêts à fournir une ventilation assistée lorsque les médicaments commencent à agir. La surveillance continue des signes vitaux doit être assurée, et la durée de chaque tentative, limitée. Il est démontré que la vidéolaryngoscopie améliore la réussite de l’intubation dès la première tentative[61][62]; ce devrait donc être la méthode privilégiée[63]. L’oxygénation apnéique au moyen d’une canule nasale à haut débit pendant le processus d’intervention, dont la fraction inspirée en oxygène correspond aux besoins du nouveau-né pendant cette période, accroît la probabilité d’intubation réussie à la premiète tentative, tout en réduisant le risque de désaturation[64]. L’installation de la canule devrait être confirmée par une démonstration du dioxyde de carbone expiré, accompagnée d’une amélioration de la fréquence cardiaque[65]. Les nouveau-nés atteints d’une anomalie respiratoire devraient être intubés par une équipe d’experts, en présence d’un otorhinolaryngologiste ou d’un anesthésiologiste, dans la mesure du possible.
Recommandations
- La prémédication devrait être administrée lors de toutes les laryngoscopies, sauf en cas d’urgence clinique (p. ex., la réanimation néonatale). Lorsqu’il est impossible d’obtenir un accès intraveineux, on peut envisager l’administration de fentanyl par voie intranasale.
- La prémédication optimale en vue de l’intubation et de l’administration de surfactant selon la technique INSURE (intuber-surfactant-extuber) devrait inclure une association de vagolytique, d’opioïde à action rapide et de relaxant musculaire à courte durée d’action. Les médicaments et les posologies suggérés s’établissent comme suit : de 0,01 mg/kg à 0,02 mg/kg d’atropine, 2 mcg/kg de fentanyl (injectés lentement sur deux à cinq minutes) et 2 mg/kg de succinylcholine. La succinylcholine est à éviter en cas d’hyperkaliémie, d’histoire familiale d’hyperthermie maligne ou de trouble neuromusculaire congénital.
- L’administration moins invasive de surfactant (LISA) et le traitement mini-invasif au surfactant (MIST) devraient inclure des mesures non pharmacologiques (p. ex., « position de regroupement » ou contention) pour gérer la douleur. En plus des mesures non pharmacologiques, il faut administrer de l’atropine avant ces deux interventions pour éviter la stimulation vagale et la bradycardie, et faire suivre cette médication d’une plus petite dose de fentanyl (1 mcg/kg injecté lentement par voie intraveineuse, sur deux à cinq minutes).
- Les données sont insuffisantes pour recommander une prémédication lors du recours à la voie supraglottique. Des protocoles semblables à ceux utilisés lors de l’intubation sont à envisager.
- Les prestataires de soins devraient connaître la pharmacocinétique des médicaments qu’ils utilisent, afin de pouvoir ajuster la posologie en cas de dysfonctionnement hépatique ou rénal. La clairance du rémifentanil est rapide dans le sang et les tissus, et par conséquent, ce médicament dépend moins du fonctionnement hépatique et rénal. On peut envisager d’administrer du rémifentanil pour remplacer le fentanyl en cas de dysfonctionnement hépatique ou rénal.
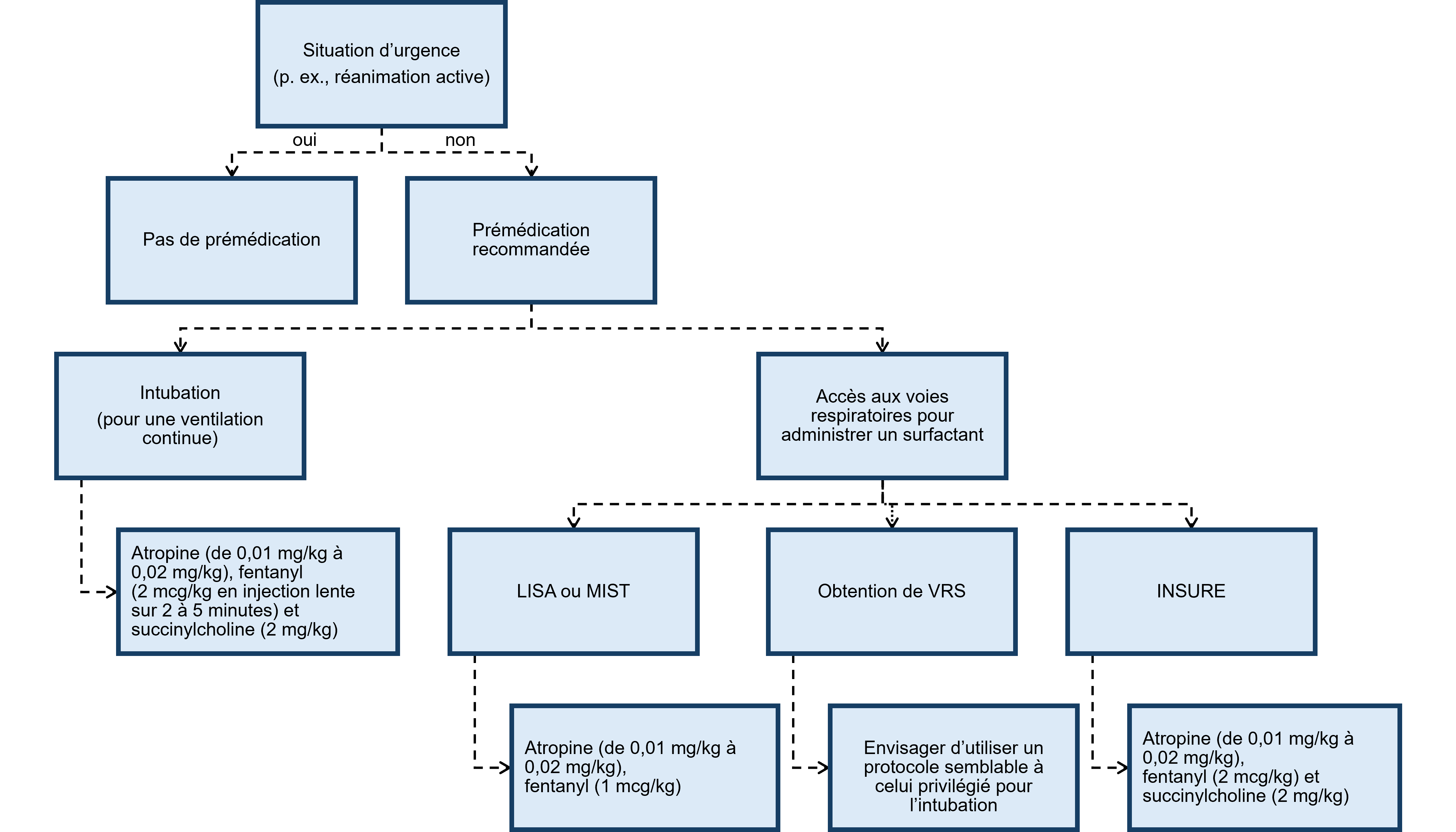
Figure 1. Organigramme d’aide à la décision lors de la prémédication
INSURE intuber-surfactant-extuber; LISA administration moins invasive de surfactant; MIST administration mini-invasive de surfactant; VSG voie supraglottique
Remerciements
Les auteurs remercient madame Charmaine De Castro, spécialiste de l’information à la Sidney Liswood Health Sciences Library du Mount Sinai Hospital de Toronto, qui a procédé à l’analyse bibliographique préalable à la rédaction du présent document. Le comité de la pédiatrie communautaire, le comité de la pharmacothérapie, le comité des soins aigus de même que le comité directeur de la section de la médecine néonatale et périnatale de la Société canadienne de pédiatrie ont révisé le présent document de principes.
COMITÉ D’ÉTUDE ET DU NOUVEAU-NÉ DE LA SOCIÉTÉ CANADIENNE DE PÉDIATRIE (2024-2025)
Membres : Souvik Mitra MD M. Sc. (président), Michael Narvey MD (président sortant), Sidd Thakore MD (représentant du conseil), Gabriel Altit MD, Nicole Radziminski MD, Emer Finan MB, Mireille Guillot MD, Frances Morin MD (membre résidente)
Représentants : William Ehman MD (Le Collège des médecins de famille du Canada), Chantal Nelson (Agence de la santé publique du Canada), Eric Eichenwald MD (American Academy of Pediatrics, comité d’étude du fœtus et du nouveau-né), Douglas Wilson MD (La Société des obstétriciens et gynécologues du Canada), Isabelle Milette inf. M. Sc. inf. ISPNN (Association canadienne des infirmières et infirmiers en néonatalogie), Deepak Manhas MD (section de la médecine néonatale et périnatale de la SCP)
Auteurs principaux : Anne-Sophie Gervais MD, Keith J. Barrington MD, Emer Finan MB
Financement
Aucun financement n’a été accordé pour la préparation du présent manuscrit.
Conflits d’intérêts potentiels
Les auteurs n’ont aucuns conflits d’intérêts à déclarer.
Références
- Caldwell CD, Watterberg KL. Effect of premedication regimen on infant pain and stress response to endotracheal intubation. J Perinatol 2015;35(6):415–8. doi : 10.1038/jp.2014.2272
- Ancora G, Lago P, Garetti E et coll. Evidence‐based clinical guidelines on analgesia and sedation in newborn infants undergoing assisted ventilation and endotracheal intubation. Acta Paediatr 2019;108(2):208–17. doi : 10.1111/apa.14606
- Venkatesh V, Ponnusamy V, Anandaraj J et coll. Endotracheal intubation in a neonatal population remains associated with a high risk of adverse events. Eur J Pediatr 2011;170(2):223–7. doi : 10.1007/s00431-010-1290-8
- Tippmann S, Kidszun A. Adequate analgesia and sedation should be given to neonates during non‐emergency endotracheal intubation. Acta Paediatr 2020;109(1):17–9. doi : 10.1111/apa.14987
- Ng E, Shah V; Société canadienne de pédiatrie, comité d’étude fœtus et du nouveau-né. Les directives pour le traitement par surfactant exogène chez le nouveau-né. Paediatr Child Health 2021;26(1):42-9. doi : 10.1093/pch/pxaa117
- Krajewski P, Szpecht D, Hożejowski R. Premedication practices for less invasive surfactant administration — results from a nationwide cohort study. J Matern Fetal Neonatal Med 2022;35(24):4750–4. doi : 10.1080/14767058.2020.1863365
- Kuek SL, Jacobs SE, Manley BJ. Sedation during minimal invasive surfactant treatment. Acta Paediatr 2020;109(8):1685–6. doi : 10.1111/apa.15228
- Balakrishnan A, Sanghera RS, Boyle EM. New techniques, new challenges—The dilemma of pain management for less invasive surfactant administration? Paediatr Neonatal Pain 2021;3(1):2–8. doi : 10.1002/pne2.12033
- Peterson J, den Boer MC, Roehr CC. To sedate or not to sedate for less invasive surfactant administration: An ethical approach. Neonatol 2021;118(6):639–46. doi : 10.1159/000519283
- Duerden EG, Grunau RE, Guo T et coll. Early procedural pain is associated with regionally-specific alterations in thalamic development in preterm neonates. J Neurosci 2018;38(4):878–86. doi : 10.1523/JNEUROSCI.0867-17.2017
- Duerden EG, Mclean MA, Chau C et coll. Neonatal pain, thalamic development and sensory processing behaviour in children born very preterm. Early Hum Dev 2022;170:105617. doi : 10.1016/j.earlhumdev.2022.105617
- Selvanathan T, Ufkes S, Guo T et coll. Pain exposure and brain connectivity in preterm infants. JAMA Netw Open 2024;7(3):e242551. doi : 10.1001/jamanetworkopen.2024.2551
- McPherson C, Grunau RE. Pharmacologic analgesia and sedation in neonates. Clin Perinatol 2022;49(1):243–65. doi : 10.1016/j.clp.2021.11.014
- Barrington K; Société canadienne de pédiatrie, comité d’étude fœtus et du nouveau-né. La prémédication en vue de l’intubation trachéale chez le nouveau-né. Paediatr Child Health. 2011;16(3):165–71. doi : 10.1093/pch/16.3.165
- Durrmeyer X, Walter-Nicolet E, Chollat C et coll. Premedication before laryngoscopy in neonates: Evidence-based statement from the French Society of Neonatology (SFN). Front Pediatr 2023;10:1075184. doi : 10.3389/fped.2022.1075184
- Bottor LT. Rapid sequence intubation in the neonate. Adv Neonatal Care 2009;9(3):111-7; quiz 118-9. doi : 10.1097/ANC.0b013e3181a68cd4
- Lemyre B, Doucette J, Kalyn A et coll. Morphine for elective endotracheal intubation in neonates: A randomized trial [ISRCTN43546373]. BMC Pediatr 2004;4(1):20. doi : 10.1186/1471-2431-4-20
- Perlman JM, Goodman S, Kreusser KL, Volpe JJ. Reduction in intraventricular hemorrhage by elimination of fluctuating cerebral blood-flow velocity in preterm infants with respiratory distress syndrome. New Engl J Med 1985;312(21):1353–7. doi : 10.1056/NEJM198505233122104
- Raju TN, Vidyasagar D, Torres C et coll. Intracranial pressure during intubation and anesthesia in infants. J Pediatr 1980;96(5):860–2. doi : 10.1016/s0022-3476(80)80558-0
- Kelly MA, Finer NN. Nasotracheal intubation in the neonate: Physiologic responses and effects of atropine and pancuronium. J Pediatr 1984;105(2):303–9. doi : 10.1016/s0022-3476(84)80137-7
- Maheshwari R, Tracy M, Badawi N, Hinder M. Neonatal endotracheal intubation: How to make it more baby friendly. J Paediatr Child Health 2016;52(5):480–6. doi : 10.1111/jpc.13192
- Marshall TA, Deeder R, Pai S et coll. Physiologic changes associated with endotracheal intubation in preterm infants. Crit Care Med 1984;12(6):501–3. doi : 10.1097/00003246-198406000-00006
- Billingham S. Rapid sequence intubation. J Neonatal Nurs 2012;18(1):25–9. doi : 10.1016/j.jnn.2010.11.001
- Badiee Z, Vakiliamini M, Mohammadizadeh M. Remifentanil for endotracheal intubation in premature infants: A randomized controlled trial. J Res Pharm Pract 2013;2(2):75–82. doi : 10.4103/2279-042X.117387
- Ozawa Y, Ades A, Foglia EE et coll. Premedication with neuromuscular blockade and sedation during neonatal intubation is associated with fewer adverse events. J Perinatol 2019;39(6):848–56. doi : 10.1038/s41372-019-0367-0
- Neches SK, Brei BK, Umoren R et coll. Association of full premedication on tracheal intubation outcomes in the neonatal intensive care unit: An observational cohort study. J Perinatol 2023;43(8):1007–14. doi : 10.1038/s41372-023-01632-5
- O’Donnell CPF, Kamlin COF, Davis PG, Morley CJ. Endotracheal intubation attempts during neonatal resuscitation: Success rates, duration, and adverse effects. Pediatrics 2006;117(1):e16-21. doi : 10.1542/peds.2005-0901
- Kumar P, Denson SE, Mancuso TJ, comité d’étude du fœtus et du nouveau-né, section de l’anesthésiologie et de la médecine de la douleur de l’AAP. Premedication for nonemergency endotracheal intubation in the neonate. Pediatrics 2010;125(3):608–15. doi : 10.1542/peds.2009-2863
- Barrington KJ, Finer NN, Etches PC. Succinylcholine and atropine for premedication of the newborn infant before nasotracheal intubation: A randomized, controlled trial. Crit Care Med 1989;17(12):1293–6. doi : 10.1097/00003246-198912000-00009
- Afifi J, El-Naggar W, Hatfield T et coll. Atropine versus placebo for neonatal nonemergent intubation: A randomized clinical trial. J Pediatr 2025;286:114719. doi : 10.1016/j.jpeds.2025.114719
- de Kort EHM, Hanff LM, Roofthooft D et coll. Insufficient sedation and severe side effects after fast administration of remifentanil during INSURE in preterm newborns. Neonatology 2017;111(2):172–6. doi : 10.1159/000450536
- McNair C, Graydon B, Taddio A. A cohort study of intranasal fentanyl for procedural pain management in neonates. Paediatr Child Health 2018;23(8):e170–5. doi : 10.1093/pch/pxy060
- Ku LC, Simmons C, Smith PB et coll. Intranasal midazolam and fentanyl for procedural sedation and analgesia in infants in the neonatal intensive care unit. J Neonatal Perinatal Med 2019;12(2):143–8. doi : 10.3233/NPM-17149
- Kaushal S, Placencia JL, Maffei SR, Chumpitazi CE. Intranasal fentanyl use in neonates. Hosp Pharm 2020;55(2):126–9. doi : 10.1177/0018578719828335
- Ghanta S, Abdel-Latif ME, Lui K et coll. Propofol compared with the morphine, atropine, and suxamethonium regimen as induction agents for neonatal endotracheal intubation: A randomized, controlled trial. Pediatrics 2007;119(6):e1248-55. doi : 10.1542/peds.2006-2708
- Durrmeyer X, Breinig S, Claris O et coll. Effect of atropine with propofol vs atropine with atracurium and sufentanil on oxygen desaturation in neonates requiring nonemergency intubation: A randomized clinical trial. JAMA 2018;319(17):1790–801. doi : 10.1001/jama.2018.3708
- Simons SHP, van der Lee R, Reiss IKM, van Weissenbruch MM. Clinical evaluation of propofol as sedative for endotracheal intubation in neonates. Acta Paediatr 2013;102(11):e487-92. doi : 10.1111/apa.12367
- de Kort EHM, Twisk JWR, van T Verlaat EPG et coll. Propofol in neonates causes a dose‐dependent profound and protracted decrease in blood pressure. Acta Paediatr 2020;109(12):2539–46. doi : 10.1111/apa.15282
- Welzing L, Kribs A, Eifinger F et coll. Propofol as an induction agent for endotracheal intubation can cause significant arterial hypotension in preterm neonates. Pediatr Anesth 2010;20(7):605–11. doi : 10.1111/j.1460-9592.2010.03330.x
- Avino D, Zhang WH, De Villé A, Johansson AB. Remifentanil versus morphine-midazolam premedication on the quality of endotracheal intubation in neonates: A noninferiority randomized trial. J Pediatr 2014;164(5):1032–7. doi : 10.1016/j.jpeds.2014.01.030
- Ng E, Taddio A, Ohlsson A. Intravenous midazolam infusion for sedation of infants in the neonatal intensive care unit. Cochrane Database Syst Rev 2017;1(1):CD002052. doi : 10.1002/14651858.CD002052.pub3
- Ng E, Klinger G, Shah V, Taddio A. Safety of benzodiazepines in newborns. Ann Pharmacother 2002;36(7–8):1150–5. doi : 10.1345/aph.1A328
- Milési C, Baleine J, Mura T et coll. Nasal midazolam vs ketamine for neonatal intubation in the delivery room: A randomised trial. Arch Dis Child Fetal Neonatal Ed 2018;103(3):F221–6. doi : 10.1136/archdischild-2017-312808
- Wilmott AR, Thompson GC, Lang E et coll. Atropine therapy versus no atropine therapy for the prevention of adverse events in paediatric patients undergoing intubation. Cochrane Database Syst Rev 2018;2018(1):CD010898. doi : 10.1002/14651858.CD010898.pub2
- Pokela ML, Koivisto M. Physiological changes, plasma beta-endorphin and cortisol responses to tracheal intubation in neonates. Acta Paediatr 1994;83(2):151–6. doi : 10.1111/j.1651-2227.1994.tb13040.x
- Truong L, Kim JH, Katheria AC et coll. Haemodynamic effects of premedication for neonatal intubation: An observational study. Arch Dis Child Fetal Neonatal Ed 2020;105(2):123–7. doi : 10.1136/archdischild-2018-316235
- Thewissen L, Caicedo A, Dereymaeker A et coll. Cerebral autoregulation and activity after propofol for endotracheal intubation in preterm neonates. Pediatr Res 2018;84(5):719–25. doi : 10.1038/s41390-018-0160-3
- Sauer CW, Kong JY, Vaucher YE et coll. Intubation attempts increase the risk for severe intraventricular hemorrhage in preterm infants—A retrospective cohort study. J Pediatr 2016;177:108–13. doi : 10.1016/j.jpeds.2016.06.051
- Cheng C, Tabbara N, Cheng C, Shah V. Intranasal fentanyl for procedural analgesia in preterm infants. Front Pain Res (Lausanne) 2022;2:815014. doi : 10.3389/fpain.2021.815014
- Baleine J, Milési C, Mesnage R et coll. Intubation in the delivery room: Experience with nasal midazolam. Early Hum Dev 2014;90(1):39–43. doi : 10.1016/j.earlhumdev.2013.10.007
- Fahnenstich H, Steffan J, Kau N, Bartmann P. Fentanyl-induced chest wall rigidity and laryngospasm in preterm and term infants. Crit Care Med 2000;28(3):836–9. doi : 10.1097/00003246-200003000-00037
- Müller P, Vogtmann C. Three cases with different presentation of fentanyl-induced muscle rigidity—A rare problem in intensive care of neonates. Am J Perinatol 2000;17(1):23–6. doi : 10.1055/s-2000-7289
- Dewhirst E, Naguib A, Tobias JD. Chest wall rigidity in two infants after low-dose fentanyl administration. Pediatr Emerg Care 2012;28(5):465–8. doi : 10.1097/PEC.0b013e3182535a2a
- Pitsiu M, Wilmer A, Bodenham A et coll. Pharmacokinetics of remifentanil and its major metabolite, remifentanil acid, in ICU patients with renal impairment. Br J Anaesth 2004;92(4):493–503. doi : 10.1093/bja/aeh086
- Elmekkawi A, Abdelgadir D, Van Dyk J et coll. Use of naloxone to minimize extubation failure after premedication for INSURE procedure in preterm neonates. J Neonatal Perinatal Med 2016;9(4):363–70. doi : 10.3233/NPM-915141
- Brahmbhatt S, Read B, Da Silva O, Bhattacharya S. A survey of minimally invasive surfactant therapy in Canada. Can J Respir Ther 2022;58:122–6. doi : 10.29390/cjrt-2022-011
- Yew R, Fleeman M, Gowda H. Should premedication be used for less invasive surfactant administration (LISA)? Arch Dis Child 2023;108(2):141-3. doi : 10.1136/archdischild-2022-324922
- Dekker J, Lopriore E, van Zanten HA et coll. Sedation during minimal invasive surfactant therapy: A randomised controlled trial. Arch Dis Child Fetal Neonatal Ed 2019;104(4):F378–83. doi : 10.1136/archdischild-2018-315015
- Sk H, Saha B, Mukherjee S, Hazra A. Premedication with fentanyl for less invasive surfactant application (LISA): A randomized controlled trial. J Trop Pediatr 2022;68(2):fmac019. doi : 10.1093/tropej/fmac019
- Roberts CT, Halibullah I, Bhatia R et coll. Outcomes after introduction of minimally invasive surfactant therapy in two Australian tertiary neonatal units. J Pediatr 2021;229:141–6. doi : 10.1016/j.jpeds.2020.10.025
- Geraghty LE, Dunne EA, Ní Chathasaigh CM et coll. Video versus direct laryngoscopy for urgent intubation of newborn infants. N Engl J Med 2024;390(20):1885-94. doi : 10.1056/NEJMoa2402785
- Moussa A, Sawyer T, Puia-Dumitrescu M et coll. Does videolaryngoscopy improve tracheal intubation first attempt success in the NICUs? A report from the NEAR4NEOS. J Perinatol 2022;42(9):1210–5. doi : 10.1038/s41372-022-01472-9
- Disma N, Asai T, Cools E et coll. Airway management in neonates and infants: European Society of Anaesthesiology and Intensive Care and British Journal of Anaesthesia joint guidelines. Eur J Anaesthesiol 2024;41(1):3–23. doi : 10.1097/EJA.0000000000001928
- Hodgson KA, Owen LS, Kamlin COF et coll. Nasal high-flow therapy during neonatal endotracheal intubation. N Engl J Med 2022;386(17):1627–37. doi : 10.1056/NEJMoa2116735
- Zaichkin J, Kamath-Rayne BD, Weiner G. The NRP 8th Edition: Innovation in Education. Adv Neonatal Care 2021;21(4):322–32. doi : 10.1097/ANC.0000000000000884
Avertissement : Les recommandations du présent document de principes ne constituent pas une démarche ou un mode de traitement exclusif. Des variations tenant compte de la situation du patient peuvent se révéler pertinentes. Les adresses Internet sont à jour au moment de la publication.