Point de pratique
La prise en charge de la dilatation des voies urinaires en période anténatale : un point de pratique clinique pour les prestataires de soins néonatals
Affichage : le 19 janvier 2026
Auteur(s) principal(aux)
Laura Betcherman MD, Charushree Prasad MD, Matt Harding MD, Robert L. Myette MD Ph. D., Peter Wong MD, Priya Saini MD; Société canadienne de pédiatrie, Comité de la pédiatrie communautaire
Résumé
La dilatation des voies urinaires en période anténatale est un scénario clinique courant en pédiatrie. En raison des diverses lignes directrices, de la variabilité des pratiques et des comptes rendus hétérogènes des échographies, il est difficile de savoir quels nouveau-nés auront besoin d’un suivi et à quel moment effectuer l’imagerie postnatale ainsi que de déterminer s’il est nécessaire d’administrer une prophylaxie antibiotique. Tant les échographies anténatales que postnatales devraient être utilisées pour évaluer le diamètre antéropostérieur du pyélon rénal et la présence de manifestations complexes. Les indications d’imagerie supplémentaire, de prophylaxies antibiotiques et de consultation en surspécialité en dépendent. Les données probantes en appui à l’utilisation d’une prophylaxie antibiotique sont limitées, mais cette utilisation peut être envisagée dans un modèle de prise de décision commune avec la famille des patients dont les manifestations cliniques sont complexes et dont la mesure du diamètre antéropostérieur du pyélon rénal est élevée. Le présent point de pratique intègre les lignes directrices déjà connues aux données probantes exemplaires pour créer un cheminement clinique afin de prendre en charge la dilatation des voies urinaires en période anténatale.
Mots-clés : dilatation des voies urinaires; hydronéphrose anténatale; obstruction de la jonction pyélo-urétérale; prophylaxie antibiotique; reflux vésico-urétéral
Contexte
La dilatation des voies urinaires (DVU) est une anomalie souvent détectée à l’échographie prénatale, qu’on observe dans jusqu’à 5 % des grossesses. Même si la plupart des cas sont transitoires, la DVU est associée à des anomalies congénitales de l’appareil rénal et des voies urinaires[1][2]. Ces affections comprennent le reflux vésico-urétéral (dans 10 % à 40 % des cas), l’obstruction de la jonction pyélo-urétérale (dans 10 % à 30 % des cas), l’obstruction de la jonction urétéro-vésicale (dans 5 % à 10 % des cas), le méga-uretère primaire (dans 5 % à 15 % des cas) et les valves urétrales postérieures (dans 1 % à 5 % des cas)[3]. Il est important de détecter et de prendre en charge la DVU rapidement pour éviter les complications, comme des infections urinaires récurrentes, la néphrolithiase et l’uropathie obstructive, qui peuvent toutes entraîner une néphropathie chronique[2]. Les DVU plus graves en période anténatale sont corrélées avec un plus fort risque de pathologie substantielle sur le plan clinique[4][5].
Les définitions d’hydronéphrose anténatale peuvent être vagues, en grande partie à cause de la grande variabilité de la terminologie descriptive. Dans le présent point de pratique, le terme DVU est préféré à hydronéphrose anténatale, car il est plus inclusif. Le diamètre antéropostérieur du pyélon rénal (DAPPR) est généralement utilisé pour stratifier la DVU, mais cette mesure peut plus ou moins fluctuer en fonction des changements physiologiques, de l’état liquidien, de la position de la sonde échographique et de la technique de l’opérateur[6]. Pour déterminer la gravité de la DVU, il faut évaluer le DAPPR conjointement avec les manifestations complexes (tableau 1)[7][8]. Il est à souligner que la dilatation hors du pyélon rénal n’est pas reliée à l’amincissement du parenchyme rénal et n’est donc pas considérée comme une manifestation complexe.
| Tableau 1. Les manifestations complexes associées à la dilatation des voies urinaires | ||
| Voies urinaires supérieures | ||
|
DVU bilatérale |
|
|
|
Rein unique accompagné d’une DVU |
|
|
|
Dysplasie(s) rénale(s) accompagnée(s) d’une DVU |
|
|
|
Dilatation pyélocalicielle |
|
|
|
Amincissement du parenchyme |
|
|
| Voies urinaires inférieures | ||
|
Anomalie de la vessie |
|
|
|
Anomalie de l’uretère |
|
|
| Fœtus | ||
|
Anomalie du liquide amniotique |
|
|
DAPPR diamètre antéropostérieur du pyélon rénal; DVU dilatation des voies urinaires; NPC néphropathie chronique; VUP valves de l’urètre postérieur
Un aperçu de lignes directrices en place
Les soins des nouveau-nés atteints d’une DVU en période anténatale comportent des difficultés parce qu’il n’existe aucune ressource irrévocable sur la prise en charge et que le suivi postnatal est très variable. Deux documents de directives majeurs tiennent compte à la fois du DAPPR et des manifestations complexes, soit les lignes directrices de l’Association des urologues du Canada et le système de classification multidisciplinaire de la DVU[9][10]. Tous deux présentent une bonne interfiabilité et une bonne intrafiabilité pour confirmer une DVU[11]. L’Association des urologues du Canada, qui définit la DVU en période anténatale à partir de la classification de la Society of Fetal Urology, tient compte à la fois du DAPPR et de la présence d’un amincissement cortical[9]. La mise à jour du système de classification de la DVU vise à définir les anomalies constatées pendant la période anténatale (A) et postnatale (P) et à attribuer des grades de gravité[8][10]. Les catégories les plus à risque (A2-3, P2-3) sont attribuées d’après un DAPPR accru conjugué à des anomalies des calices, de l’uretère, de la vessie et du parenchyme rénal[8][10]. Les deux systèmes de classification peuvent contribuer à la prise en charge de la DVU postnatale, mais ils comportent des divergences pour ce qui est des comptes rendus des radiographies sur les manifestations complexes. Ces disparités peuvent provoquer des difficultés d’interprétation et de communication chez les prestataires de soins, de même que lors de l’analyse des résultats des interventions chirurgicales et des recherches chez les patients[8][9].
En 2025, l’American Academy of Pediatrics a publié de nouvelles lignes directrices, en anglais, et adapté ses recommandations à partir du système de classification de la DVU, lesquelles sont généralement conformes à celles du présent point de pratique de la Société canadienne de pédiatrie[12]. Notamment, les deux documents visent à limiter la prise d’antibiotiques et à adapter la prise en charge individuelle en fonction de la présence ou de l’absence de traits caractéristiques supplémentaires et du diamètre antéropostérieur au moment de traiter les nouveau-nés ayant une DVU.
La prophylaxie antibiotique
La prophylaxie antibiotique continue (PAC) est utilisée pour limiter l’incidence d’infections urinaires chez les enfants ayant une DVU. Selon le principe sous-jacent de ce traitement, la stase et le reflux urinaires sont moins susceptibles d’être responsables d’infections urinaires lorsque l’urine est stérile[13]. La PAC comporte des désavantages : les effets secondaires, le coût, le fardeau lié à la prise de comprimés et le risque d’antibiorésistance. Les recommandations reposent largement sur un consensus d’experts, et jusqu’à présent, aucune donnée probante solide n’en soutient l’utilisation.
Une analyse systématique de l’Association des urologues du Canada réalisée en 2013 n’a établi aucun avantage à la PAC en cas de faible grade d’hydronéphrose (SFU 1-2), mais à un grade plus élevé (SFU 3-4), les nouveau-nés qui en prennent courent un risque d’infection urinaire beaucoup plus faible (14,6 %) que ceux qui n’en prennent pas (28,9 %, P<0,01)[14]. D’après une analyse subséquente effectuée en 2017, il n’y avait pas de différence significative de réduction des taux d’infection urinaire à tous les grades d’hydronéphrose[13]. Cependant, des variables importantes tirées des deux études, comme le genre, le reflux et la circoncision, ne faisaient pas l’objet d’une analyse rigoureuse[13][14], ce qui risque d’en limiter l’applicabilité dans les groupes à haut risque.
Une analyse systématique récente de l’European Society for Paediatric Urology a relevé des données insuffisantes pour appuyer l’utilisation régulière de la PAC chez les nouveau-nés ayant une DVU, mais a déterminé que cette médication pourrait comporter des avantages dans des sous-groupes particuliers (garçons non circoncis, hydro-urétéronéphrose, DVU de grade élevé)[15]. Selon une étude randomisée et contrôlée de 2023 chez les nouveau-nés ayant un reflux vésiculo-urétéral de grade 3 à 5 sans infection urinaire antérieure, l’utilisation régulière de PAC n’est pas justifiée, mais pourrait être bénéfique chez les patientes ayant un reflux vésiculo-urétéral de grade 4 ou 5[16]. Dans cette étude, la PAC était associée tant à une augmentation de l’incidence d’infections urinaires non liées à l’E. coli qu’à une augmentation de l’antibiorésistance (52 % par rapport à 17 %)[16].
La réduction du fardeau des infections urinaires et des séquelles qui en découlent est généralement citée pour justifier une PAC. Cependant, une analyse systématique a démontré que la PAC n’avait aucune influence sur la prévention des cicatrices rénales chez les enfants atteints d’infections urinaires récurrentes, même si les auteurs n’étaient pas en mesure d’en commenter l’utilité chez les patients présentant un reflux de haut grade, une dysplasie rénale ou ces deux affections[17].
Dans l’ensemble, puisque les données ne réussissent pas à démontrer d’avantages marqués à la PAC, mais qu’elles accroissent les inquiétudes d’antibiorésistance, les données probantes à jour n’appuient pas l’utilisation régulière de la PAC pour traiter la DVU. Lorsque le tableau clinique est bénin (p. ex., DAPPR maximal de 14 mm sans manifestations complexes), les parents devraient être informés des symptômes d’infection urinaire et des situations dans lesquelles consulter. Plus de données devront être amassées pour prendre en charge les nouveau-nés ayant une DVU grave, qu’ils présentent ou non des facteurs de risque supplémentaires d’infection urinaire. Chez les patients à haut risque (p. ex., un DAPPR de 15 mm ou plus ou des manifestations plus complexes), les décisions relatives à un traitement par PAC conjugué à une consultation auprès de surspécialistes devraient être prises en commun avec la famille. Les patients chez qui on soupçonne une obstruction de la jonction pyélo-urétérale n’ont pas nécessairement besoin d’une PAC, mais il est raisonnable d’entreprendre une prophylaxie en présence d’un grade élevé de DVU, dans l’attente d’une consultation en surspécialité.
La triméthoprime (sans sulfaméthoxazole) est la PAC la plus utilisée, à une dose recommandée de 2 mg/kg/jour[15]. La céphalexine et la nitrofurantoïne peuvent la remplacer. L’administration de triméthoprime-sulfaméthoxazole aux nourrisons de moins de deux mois accroît le risque d’ictère[9]. La nitrofurantoïne chez les nouveau-nés de moins d’un mois peut être responsable d’une anémie hémolytique[9]. Il faut consulter les antibiogrammes locaux pour sélectionner un médicament approprié.
Le cheminement clinique
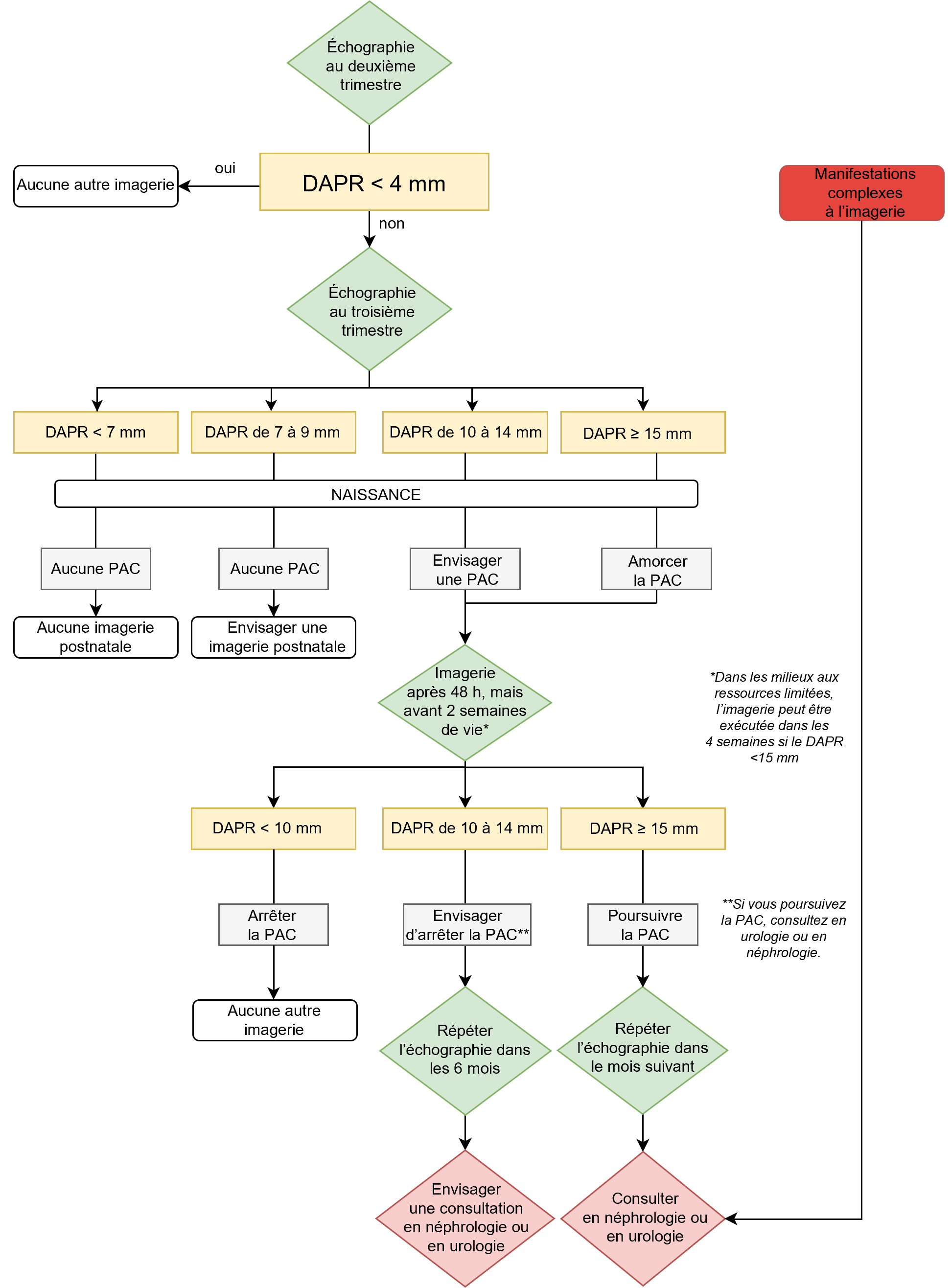
Le cheminement clinique suivant est recommandé d’après un consensus d’experts et l’utilisation du système de classification de la DVU en guise de référence afin de tenir compte à la fois du DAPPR et des manifestations complexes (figure 1). Les prestataires de soins devraient prodiguer des conseils aux familles quant aux signes et symptômes d’infection urinaire chez les nouveau-nés et quant au moment de consulter un médecin. Ce cheminement clinique fait ressortir l’importance d’une échographie postnatale de suivi chez les patients ayant une DVU en période anténatale. Le risque d’uropathologie est faible lorsque le DAPPR fœtal est de 7 mm à 9 mm au troisième trimestre, mais certaines lignes directrices préconisent une échographie postnatale de suivi[9][10]. Un suivi peut être envisagé en fonction de l’accès aux ressources et des pratiques locales.
Figure 1. La prise en charge de la dilatation des voies urinaires en période anténatale
Remarque : Les manifestations complexes incluent une anomalie de l’uretère, une anomalie vésicale, une dilatation pyélocalicielle, un oligoamnios, un amincissement du parenchyme, une dysplasie ou une échogénicité rénale, une DVU bilatérale et une DVU dans un rein unique.
DAPPR diamètre antéropostérieur du pyélon rénal; DVU dilatation des voies urinaires; PAC prophylaxie antibiotique continue
Le moment de l’imagerie de suivi
En général, une échographie devrait être effectuée au moins 48 heures après la naissance pour éviter de sous-estimer la DVU pendant une période d’hypovolémie relative. Dans l’idéal, l’échographie est effectuée dans les deux semaines suivant la naissance. Lorsque l’accès à l’échographie est limité, la première imagerie peut être exécutée dans le mois suivant la naissance, pourvu que le DAPPR effectué au troisième trimestre soit inférieur à 15 mm et qu’aucune manifestation complexe ne soit observée.
En l’absence de telles manifestations, lorsque le DAPPR est demeuré entre 10 mm et 14 mm après la naissance, le nouveau-né peut être suivi par un praticien général, et une échographie peut être réalisée avant l’âge de six mois. Lorsque le DAPPR postnatal est de 15 mm ou plus, une reprise de l’échographie devrait être réalisée dans un délai d’un mois, et une imagerie additionnelle (cystographie ou scintigraphie rénale au Lasix) peut être envisagée parallèlement à une consultation en urologie ou en néphrologie. Si, en tout temps, la présence ou l’absence d’une manifestation complexe n’est pas indiquée dans le rapport de l’échographie et risque d’en modifier la prise en charge, le prestataire de soins peut demander des précisions en radiologie.
Une imagerie postnatale qui soulève des soupçons de valves de l’urètre postérieur pendant la période anténatale (hydro-urétérénéphrose bilatérale grave accompagnée ou non d’anomalies vésicales, modifications du parenchyme rénal, oligoamnios ou présence d’un signe « en trou de serrure ») devrait être effectuée d’urgence en consultation avec l’urologie pédiatrique. Les vidanges postnatales observées n’écartent pas un diagnostic de grave obstruction[7].
Les indications d’une consultation en néphrologie ou en urologie
Les indications particulières d’une consultation en urologie ou en néphrologie sont des manifestations complexes à l’imagerie, une DVU postnatale qui persiste ou s’aggrave, le maintien de la PAC postnatale ou un DAPPR postnatal de 15 mm ou plus.
Les indications de bilan sanguin
Les examens des électrolytes et de la fonction rénale ne sont pas indiqués en cas de DVU non complexes, mais devraient être effectués chez les nouveau-nés ayant une DVU bilatérale marquée qui laisse supposer une compression du parenchyme rénal ou qui soulève des craintes de valves de l’urètre postérieur. Le bilan sanguin devrait également être obtenu chez les nouveau-nés atteints d’une néphropathie bilatérale (p. ex., kystes bilatéraux, échogénicité accrue ou dysplasie).
Points de pratique exemplaires
- Il est important de détecter les nouveau-nés qui ont besoin d’être soumis à un suivi de la dilatation des voies urinaires (DVU) pour éviter les complications.
- La figure 1 oriente le moment de l’imagerie postnatale chez les nouveau-nés dont l’échographie anténatale révèle une DVU reliée à un diamètre antéropostérieur du pyélon rénal supérieur à 10 mm, des manifestations complexes ou ces deux problèmes.
- Les familles doivent recevoir plus de directives concrètes sur la prophylaxie antibiotique continue de leur nouveau-né, particulièrement s’il présente une DVU de grade élevé. Un modèle de décision commune est à privilégier avec la famille lors des échanges sur la prophylaxie antibiotique continue.
- Les cliniciens devraient obtenir de l’information en radiologie sur les manifestations complexes si elles ne sont pas incluses dans le compte rendu original de l’échographie.
- Le nouveau-né peut être dirigé en néphrologie pédiatrique, en urologie pédiatrique ou auprès de ces deux surspécialités s’il présente une DVU (y compris par les prestataires de soins de la mère), mais tout particulièrement en présence de manifestations complexes.
Remerciements
Les auteurs tiennent à remercier le docteur Kourosh Afshar (urologue, B.C. Children’s Hospital, Université de la Colombie-Britannique) et l’Association des néphrologues pédiatriques du Canada pour leur apport et leurs commentaires. Des membres de cette Association et du groupe d’intérêt en néphrologie de la Société canadienne de pédiatrie ont évalué et modifié le cheminement clinique. Le comité d’étude du fœtus et du nouveau-né et le comité des maladies infectieuses et d’immunisation de la Société canadienne de pédiatrie ont révisé le présent point de pratique.
COMITÉ DE LA PÉDIATRIE COMMUNAUTAIRE DE LA SOCIÉTÉ CANADIENNE DE PÉDIATRIE (2023-2024)
Membres : Peter Wong MD (président), Jill Borland Starkes MD (représentante du conseil), Audrey Lafontaine MD, Michael Hill MD, Meta van den Heuvel MD, Kelcie Lahey MD M. Sc.
Représentante : Richa Agnihotri MD (section de la pédiatrie communautaire)
Auteurs principaux : Laura Betcherman MD, Charushree Prasad MD, Matt Harding MD, Robert L. Myette MD Ph. D., Peter Wong MD, Priya Saini MD
Financement
Aucun financement n’a été accordé pour la préparation du présent manuscrit.
Conflits d’intérêts potentiels
Aucun auteur n’a de conflits d’intérêts à déclarer. Les auteurs ont remis le formulaire de divulgation des conflits d’intérêts potentiels de l’International Committee of Medical Journal Editors.
Références
- Melo FF, Mak RH, Simões E Silva AC et coll. Evaluation of urinary tract dilation classification system for prediction of long-term outcomes in isolated antenatal hydronephrosis: A cohort study. J Urol 2021;206(4):1022-30. doi : 10.1097/JU.0000000000001899
- Lee RS, Cendron M, Kinnamon DD, Nguyen HT. Antenatal hydronephrosis as a predictor of postnatal outcome: A meta-analysis. Pediatrics 2006;118(2):586-93. doi : 10.1542/peds.2006-0120
- Vincent K, Murphy HJ, Twombley KE. Urinary tract dilation in the fetus and neonate. Neoreviews 2022;23(3):e159-74. doi : 10.1542/neo.23-3-e159
- Rickard M, Dos Santos J, Keunen J, Lorenzo AJ. Prenatal hydronephrosis: Bridging pre- and postnatal management. Prenat Diagn 2022;42(9):1081-93. doi : 10.1002/pd.6114
- Hwang J, Kim PH, Yoon HM et coll. Application of the postnatal urinary tract dilation classification system to predict the need for surgical intervention among neonates and young infants. Ultrasonography 2023;42(1):136-46. doi : 10.14366/usg.22035
- Dos Santos JR, Zu’bi F, Hojjat A et coll. The impact of the state of hydration on the degree of hydronephrosis in children: Towards a uniform standard of ultrasonographic assessment. Pediatrics 2018;141 (1_MeetingAbstract):283.
- Coquillette M, Lee RS, Pagni SE, Cataltepe S, Stein DR. Renal outcomes of neonates with early presentation of posterior urethral valves: A 10-year single center experience. J Perinatol 2020;40(1):112-7. doi : 10.1038/s41372-019-0489-4
- Nguyen HT, Phelps A, Coley B, Darge K, Rhee A, Chow JS. 2021 update on the urinary tract dilation (UTD) classification system: Clarifications, review of the literature, and practical suggestions. Pediatr Radiol 2022;52(4):740-51. doi : 10.1007/s00247-021-05263-w
- Capolicchio JP, Braga LH, Szymanski KM. Canadian Urological Association/Pediatric Urologists of Canada guideline on the investigation and management of antenatally detected hydronephrosis. Can Urol Assoc J 2018;12(4):85–92. doi : 10.5489/cuaj.5094
- Nguyen HT, Benson CB, Bromley B et coll. Multidisciplinary consensus on the classification of prenatal and postnatal urinary tract dilation (UTD classification system). J Pediatr Urol 2014;10(6):982–98. doi : 10.1016/j.jpurol.2014.10.002
- Rickard M, Easterbrook B, Kim S et coll. Six of one, half a dozen of the other: A measure of multidisciplinary inter/intra-rater reliability of the Society for Fetal Urology and urinary tract dilation grading systems for hydronephrosis. J Pediatr Urol 2017;13(1):80.e1-5. doi : 10.1016/j.jpurol.2016.09.005
- Herndon CDA, Otero HJ, Hains D, Sweeney RM, Lockwood GM, sections d’urologie, de néphrologie, de radiologie et de médecine hospitalière de l’American Academy of Pediatrics. Perinatal urinary tract dilation: Recommendations on pre-/postnatal imaging, prophylactic antibiotics, and follow-up; Clinical report. Pediatrics 2025;156(1):e2025071814. doi : 10.1542/peds.2025-071814
- Easterbrook B, Capolicchio JP, Braga LH. Antibiotic prophylaxis for prevention of urinary tract infections in prenatal hydronephrosis: An updated systematic review. Can Urol Assoc J 2017;11(1-2Suppl1):S3-11. doi : 10.5489/cuaj.4384
- Braga LH, Mijovic H, Farrokhyar F, Pemberton J, DeMaria J, Lorenzo AJ. Antibiotic prophylaxis for urinary tract infections in antenatal hydronephrosis. Pediatrics 2013;131(1):e251-61. doi : 10.1541/peds.2012-1870
- Silay MS, Undre S, Nambiar AK et coll. Role of antibiotic prophylaxis in antenatal hydronephrosis: A systematic review from the European Association of Urology/European Society for Paediatric Urology Guidelines Panel. J Pediatr Urol 2017;13(3):306-15. doi : 10.1016/j.jpurol.2017.02.023
- Morello W, Baskin E, Jankauskiene A et coll; groupe d’étude PREDICT. Antibiotic prophylaxis in infants with grade III, IV, or V vesicoureteral reflux. N Engl J Med 2023;389(11):987-97. doi : 10.1056/NEJMoa2300161
- Hewitt IK, Pennesi M, Morello W, Ronfani L, Montini G. Antibiotic prophylaxis for urinary tract infection–related renal scarring: A systematic review. Pediatrics 2017;139(5):e20163145. doi : 10.1542/peds.2016-3145
Avertissement : Les recommandations du présent document de principes ne constituent pas une démarche ou un mode de traitement exclusif. Des variations tenant compte de la situation du patient peuvent se révéler pertinentes. Les adresses Internet sont à jour au moment de la publication.